Microsoft Word - informator 2015-priprema.doc
|
|
|
- Лиле Кнежевић
- пре 5 година
- Прикази:
Транскрипт
1 ИНФОРМАТОР 29 UNIVERZITET U BEOGRADU jun godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Hemijska svojstva elemenata određuje: A. odnos izotopa u elementu D. broj energetskih podnivoa B. masa atoma E. broj valentnih elektrona C. broj energetskih nivoa N. ne znam (3) 2. Koja od sledećih elektronskih konfiguracija odgovara elementu 14 grupe (IVa podgrupe) Periodnog sistema elemenata? A. 1s 2 2s 2 2p 6 3s 2 3p 1 D. 1s 2 2s 2 2p 6 3s 2 3p 2 B. 1s 2 2s 2 2p 6 3s 2 3p 4 E. 1s 2 2s 2 2p 6 3s 2 3p 3 C. 1s 2 2s 2 2p 6 3s 2 3p 5 N. ne znam (3) 3. Izračunati molarnu koncentraciju 42 % rastvora azotne kiseline (HNO 3 ) čija je gustina 1,25 g/cm 3. Podaci: A r (N) = 14; A r (O) = 16; A r (H) = 1 A. 0,667 mol/dm 3 D. 47 mol/dm 3 B. 8,33 mol/dm 3 E. 98 mol/dm 3 C. 12,6 mol/dm 3 N. ne znam (8) 4. U koliko grama vode treba rastvoriti 126 g Na 2 SO 3 7 H 2 O da bi se dobio 10 % rastvor? Podaci: A r (Na) = 23; A r (S) = 32; A r (O) = 16; A r (H) = 1; A. 567 D.1134 B. 504 E C. 630 N. ne znam (8) 5. Koje od navedenih jedinjenja ne hidrolizuje u vodenom rastvoru? A. K 2 CO 3 D. KCN B. KCH 3 COO E. NH 4 Cl C. K 2 SO 4 N. ne znam (4)
2 30 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 6. U kom od navedenih jedinjenja azot ima oksidacioni broj III? A. NH 3 D. Ca(NO 2 ) 2 B. N 2 O 5 E. N 2 H 4 C. NH 4 NO 3 N. ne znam (4) 7. Koji od navedenih oksida je bazni oksid? A. Al 2 O 3 D. NO B. MgO E. CO 2 C. ZnO N. ne znam (3) 8. Po protolitičkoj teoriji u jednom od navedenih nizova nalaze se samo kiseline: A. NH + 4, HCl, H 3 O + D. PO 3-4, HPO , H 2 PO 4 B. CH 3 COO -, H 2 PO - - 3, HSO 4 E. H 3 O +, HCO - 2-3, CO 3 C. CN -, OH - +, NH 4 N. ne znam (3) 9. U jednačini: K 2 Cr 2 O 7 + H 2 S + H 2 SO 4 S + Cr 2 (SO 4 ) 3 + K 2 SO 4 + H 2 O stehiometrijski koeficijenti K 2 Cr 2 O 7, H 2 S i H 2 SO 4 su navedeni redom: A. 2, 3, 7 D. 1, 3, 8 B. 1, 3, 4 E. 2, 3, 8 C. 3, 3, 10 N. ne znam (7) 10. Elementarni sumpor sastoji se od molekula S 8. U 2,56 g elementarnog sumpora nalazi se: Podaci: A r (S) = 32 A. 6, molekula D. 0,470 molekula B. 0,05 molekula E. 6, molekula C. 6, molekula N. ne znam (5) 11. U 250 cm 3 rastvora nalazi se 1, OH - jona. ph-vrednost ovog rastvora iznosi: A. 9,0 D. 3,9 B. 7,0 E. 14,0 C. 4,6 N. ne znam (7) 12. Zapremina vodonika koja se, na normalnim uslovima, izdvoji u reakciji HCl sa 1,35 g Al iznosi: Podaci: A r (Al) = 27 A. 3,36 dm 3 D. 1,68 dm 3 B. 1,12 dm 3 E. 22,4 dm 3 C. 11,2 dm 3 N. ne znam (5)
3 ИНФОРМАТОР Za neutralizaciju 20 cm 3 rastvora NaOH koncentracije 0,80 mol/dm 3 potrebno je 25 cm 3 rastvora sumporne kiseline, koncentracije: A mol/dm 3 D. 0,64 mol/dm 3 B. 0,032 mol/dm 3 E. 0,32 mol/dm 3 C. 0,16 mol/dm 3 N. ne znam (5) 14. Organska tečnost P, molekulske formule C 2 H 6 O, blagom oksidacijom prelazi u aldehid R molekulske formule C 2 H 4 O, a daljom oksidacijom nastaje kiselina S molekulske formule C 2 H 4 O 2. P i R zajedno u prisustvu anhidrovanog kalcijum-hlorida daju acetal T molekulske formule C 6 H 14 O 2. P i S reaguju i daju estar Z molekulske formule C 4 H 8 O 2. Jedinjenje P je: A. etanol D. metoksimetan B. etanal E. etil-etanoat C. etanska kiselina N. ne znam (8) 15. Koje od navedenih jedinjenja je optički aktivno? A. CH 3 CH 2 CH=CH 2 D. CH 3 CH 2 COOH H H H CH 3 B. H 3 C C C CH 3 E. H 3 C C C CH 2 H Cl H C. CH 3 CH 2 CONH 2 N. ne znam (5) 16. Koliko se dm 3 propena dobija (pri normalnim uslovima) dehidratacijom 30 g 2-propanola u prisustvu sumporne kiseline: Podaci: A r (C) = 12; A r (H) = 1; A r (O) = 16; A. 5,6 D. 11,2 B. 33,6 E. 22,4 C. 10 N. ne znam (6) 17. Disaharidi nastaju iz monosaharida građenjem: A. glikozidne veze uz izdvajanje vodonika B. estarske veze uz izdvajanje vode C. glikozidne veze uz izdvajanje vode D. poluacetalne veze uz izdvajanje vode E. glikozidne veze uz izdvajanje kiseonika N. ne znam (5)
4 32 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 18. Reakcijom karboksilne grupe jedne sa amino-grupom druge α-aminokiseline nastaje: A. dipeptid D. anhidrid B. estar E. keton C. etar N. ne znam (4) 19. Prema IUPAC-ovoj nomenklaturi naziv jedinjenja čija je strukturna formula CH 3 CH 2 H C C CH 3 CH je: A. 3-metil-2-pentin D. 1-heksin B. 3-metil-3-pentin E. 3-metil-1-pentin C. 3-metil-4-pentin N. ne znam (4) 20. Proces građenja sapuna je: A. redukcija D. halogenovanje B. saponifikacija E. oksidacija C. hidrogenizacija N. ne znam (3) UNIVERZITET U BEOGRADU septembar godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena Šta je zajedničko za sledeće atome: 54 Xe 138, 56 Ba 139, 57 La? A. broj protona u jezgru D. broj neutrona u jezgru B. broj elektrona u omotaču E. ništa C. broj protona i neutrona u jezgru N. ne znam (3)
5 ИНФОРМАТОР U kojoj periodi i grupi se nalazi element koji ima elektronsku konfiguraciju spoljašnjeg energetskog nivoa 4s 2 3d 6? A. 4. perioda i 2 (IIa )grupa D. 4 perioda i 6 (VIb) grupa B. 5 perioda i 8 (VIIIb )grupa E. 4 perioda i 8 (VIIIb) grupa C. 5 perioda i 5 (Vb )grupa N. ne znam (3) 3. Odrediti maseni udeo, u procentima, rastvora fosforne kiseline (H 3 PO 4 ) koncentracije 0,22 mol/dm 3 čija je gustina 1,00 g/cm 3. Podaci: A r (P) = 31; A r (O) = 16; A r (H) = 1 A. 2,16 D. 49,7 B. 4,97 E. 63 C. 27 N. ne znam (8) 4. ph vrednost rastvora hlorovodonične kiseline je 2,0. Izračunati broj vodonik- -jona u 100 cm 3 rastvora ove kiseline. A. 6, D. 6, B. 2,15 E. 6, C. 4,20 N. ne znam (5) 5. Koje od navedenih jedinjenja hidrolizuje u vodenom rastvoru? A. NaCl D. K 2 SO 4 B. NH 4 Cl E. CaCl 2 C. KNO 3 N. ne znam (4) 6. Oksidacioni brojevi mangana u MnO 4 2-, ugljenika u CO i vodonika u NaH su: A. VII, II, I D. VI, II, -I B. VII, IV, I E. VII, II, -I C. VI, IV, -I N. ne znam (4) 7. U kom jedinjenju ne postoje uslovi za stvaranje vodoničnih veza? A. HCl D. H 2 O B. C 2 H 5 OH E. HF C. NH 3 N. ne znam (3) 8. Koji od navedenih oksida je kiseli oksid? A. K 2 O D. N 2 O 5 B. CaO E. Na 2 O C. Cr 2 O 3 N. ne znam (3)
6 34 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 9. U jednačini: KMnO 4 + H 2 O 2 + H 2 SO 4 MnSO 4 + K 2 SO 4 + H 2 O + O 2 stehiometrijski koeficijenti KMnO 4, H 2 O 2 i H 2 SO 4 su navedeni redom: A. 2, 3, 5 D. 1, 5, 8 B. 2, 5, 3 E. 2, 5, 8 C. 1, 2, 6 N. ne znam (8) 10. U rastvor koji sadrži 3,7 g kalcijum-hidroksida uvedeno je 2,64 g CO 2. Izračunati masu nastalog taloga kalcijum-karbonata: Podaci: A r (Ca) = 40; A r (O) = 16; A r (C) = 12 A. 50 g D. 0,05 kg B. 5,0 g E. 0,10 kg C. 6,34 g N. ne znam (7) 11. Izračunati zapreminu vodonika, koji se pri normalnim uslovima izdvaja dejstvom razblažene sumporne kiseline na 3,27 g cinka. Podaci: A r (Zn) = 65,4 A. 560 cm 3 D. 1,12 cm 3 B. 1,12 dm 3 E. 9 dm 3 C. 11,2 dm 3 N. ne znam (5) 12. Rastvorljivost barijum-karbonata u vodi je 1,973 mg/100 cm 3. Izračunati proizvod rastvorljivosti ove soli. Podaci: A r (Ba) = 137,3; A r (O) = 16; A r (C) = 12 A. 1, D. 7, B. 1, E. 8, C. 8, N. ne znam (7) 13. Koliko se atoma kiseonika nalazi u 33,6 dm 3 tog gasa pri normalnim uslovima? A. 1, D. 1, B. 9, E. 6, C. 1,339 N. ne znam (5) 14. Na 5,6 g alkena P adira se 16 g broma. Katalitičkom hidrogenizacijom alkena P nastaje zasićeni ugljovodonik R, koji u svom molekulu nema sekundarnih C-atoma. Alken P je: Podaci: A r (Br) = 80, A r (C) = 12, A r (H) = 1 A. 2-metilpropen D. 2,3-dimetil-1-buten B. 2-buten E. 2-metilpropan C. 1-buten N. ne znam (8)
7 ИНФОРМАТОР Jedinjenje koje sa etil-magnezijum-bromidom daje 2-butanol, a redukuje Fehling-ov rastvor je: A. propanon D. propanska kiselina B. metanska kiselina E. metanol C. etanal N. ne znam (6) 16. Koji od navedenih šećera je homodisaharid: A. laktoza D. maltoza B. saharoza E. fruktoza C. glukoza N. ne znam (5) 17. Reakcijom anhidrida karboksilne kiseline i amonijaka (amonoliza) nastaje: A. amonijum-so D. keton B. estar E. amid C. sekundarni amin N. ne znam (5) 18. Kada je za neki protein poznata sekvenca (redosled) aminokiselina u polipeptidnom nizu i položaj disulfidnih mostova, definisana je njegova: A. sekundarna struktura D. kvaternerna struktura B. primarna struktura E. konformacija C. tercijarna struktura N. ne znam (4) 19. Zamenom jednog ili više vodonikovih atoma u molekulima ugljovodonika atomima halogena nastaju: A. alkil- i aril-halogenidi D. alkeni B. hloridi kiselina E. alkadieni C. alkini N. ne znam (4) 20. Masti i ulja su: A. etri D. amidi B. estri E. acil-halogenidi C. anhidridi N. ne znam (3)
8 36 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ
9 ИНФОРМАТОР 37
10 38 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ
11 ИНФОРМАТОР 39
12 40 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ
13 ИНФОРМАТОР 41
14 42 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ
15 ИНФОРМАТОР 43
16 44 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ UNIVERZITET U BEOGRADU 30. jun godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Litijum hipohlorit ima sledeću hemijsku formulu: A. LiCl D. Li 2 ClO 4 B. LiClO E. LiClO 4 C. LiClO 3 N. ne znam (3) 2. Fosfor ima redni broj 15 (Z = 15), a njegova relativna atomska masa je 31 (A r = 31). Atom fosfora sadrži: A. 15 neutrona D. 15 elektrona B. 31 elektron E. 31 proton C. 31 neutron N. ne znam (3) 3. Pri oksidaciji nekog elementa taj element: A. prima elektrone D. obrazuje kovalentnu vezu B. otpušta protone E. otpušta elektrone C. ne menja se N. ne znam (3) 4. Element čiji je hemijski simbol Co spada u: A. alkalne metale D. zemnoalkalne metale B. halogene elemente E. metaloide C. prelazne elemente N. ne znam (4) 5. U kojem od sledećih jedinjenja sumpor ima oksidacioni broj II? A. Na 2 SO 3 D. BaSO 4 B. K 2 S 2 O 7 E. NaHS C. (NH 4 ) 2 S 2 O 8 N. ne znam (4)
17 ИНФОРМАТОР Navedene su jednačine različitih hemijskih reakcija. Zaokružite onu koja predstavlja reakciju oksido redukcije. A. Cu + + CN CuCN B. Ca + 2 H 2 O Ca(OH) 2 + H 2 C. Zn(OH) HCl ZnCl H 2 O D. Mg(H 2 PO 4 ) 2 + H 2 SO 4 MgSO H 3 PO 4 E. N 2 O 5 + H 2 O 2 HNO 3 N. ne znam (5) 7. Koje od navedenih jedinjenja ne gradi vodonične veze? A. CH 4 D. H 3 PO 4 B. NH 3 E. HF C. H 2 O N. ne znam (5) 8. Koji od navedenih oksida pri rastvaranju u vodi gradi bazu? A. N 2 O 5 D. K 2 O B. SO 2 E. N 2 O C. CO N. ne znam (5) 9. Na raspolaganju su vodeni rastvori srebro nitrata i kalcijum nitrata. Ta dva rastvora se najlakše mogu razlikovati na osnovu: A. boje D. reakcije sa rastvorom H 2 O 2 B. gustine E. reakcije sa rastvorom BaCl 2 C. reakcije sa kiseonikom N. ne znam (5) 10. Beli fosfor se sastoji od molekula P 4. U 18,53 g belog fosfora nalazi se: Podaci: A r (P) = 31 A. 3, molekula D molekula B. 9, molekula E. 2, molekula C. 5, molekula N. ne znam (5) 11. Koncentracija jona OH u rastvoru iznosi 0,001 mol dm 3. Vrednost ph ovog rastvora je: A. 3 D. 11 B. 7 E. 9 C. 0,1 N. ne znam (7)
18 46 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 12. Koncentracija (količinska) rastvora natrijum-sulfata koji sadrži 28,4 g Na 2 SO 4 u 0,2 dm 3 rastvora je: Podaci: A r (Na) = 23; A r (S) = 32; A r (O) = 16 A. 65 % D. 2 mol dm 3 B. 0,2 % E. 65 mol dm 3 C. 1 mol dm 3 N. ne znam (8) 13. Izračunati masu ugljenika koja je potrebna za potpuno prevođenje 480 g Fe 2 O 3 u elementarno gvožđe reakcijom: Fe 2 O 3 (s) + 3 C(s) 2 Fe(s) + 3 CO(g) Podaci: A r (Fe) = 56; A r (O) = 16; A r (C) = 12 A. 10,8 kg D. 240 g B. 108 g E. 2,40 kg C. 48,0 g N. ne znam (8) 14. Karbociklična organska jedinjenja imaju molekulske strukture sa: A. prstenovima bez C-atoma B. otvorenim i račvastim nizovima C-atoma C. otvorenim nizovima C-atoma D. prstenovima od C-atoma i atoma drugih elemenata E. prstenovima isključivo od C-atoma N. ne znam (3) 15. Koja se od navedenih reakcija naziva saponifikacija? A. hidroliza estra u kiseloj sredini B. alkalna hidroliza estra C. transesterifikacija D. amonoliza estra E. hidroliza acil-halogenida N. ne znam (4) 16. Bromovanjem fenola nastaje: A. anilin D. benzil-alkohol B. benzil-bromid E. brombenzen C. 2,4,6-tribromfenol N. ne znam (5)
19 ИНФОРМАТОР Koje od navedenih jedinjenja sadrži asimetričan (hiralan) ugljenikov atom: A. CH 3 CH 2 CH 3 D. CH 3 Br COOH H B. H C OH E. H C H CH 3 H C. CH 2 Cl 2 N. ne znam (4) 18. Ciklobutan reaguje sa vodonikom u prisustvu nikla (katalizator) na temperaturi iznad 200 C, pri čemu nastaje: A. metan D. 1-buten B. etan E. butan C. ciklopropan N. ne znam (5) 19. Kada se etin uvodi u amonijačni rastvor srebro-nitrata, taloži se: A. Ag C C Ag D. etanol B. Cu C C Cu E. acetilen C. eten N. ne znam (6) 20. Kada se na jodmetan u apsolutnom etru deluje opiljcima magnezijuma, a zatim se u reakcionu smešu uvede ugljenik(iv)-oksid, daljom hidrolizom reakcione smeše nastaje jedinjenje A. Reakcijom jedinjenja A sa natrijumhidroksidom nastaje: A. etanal D. natrijum-acetat B. sirćetna kiselina E. natrijum-formijat C. etanol N. ne znam (8)
20 48 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ UNIVERZITET U BEOGRADU 03. septembar godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Niz sledećih hemijskih elemenata: kalaj, azot, srebro, živa, brom, predstavljen je hemijskim simbolima A. Ca, Ac, Sc, Zn, Br D. K, Ac, Sr, I, Bi B. K, At, Ag, Zr, B E. Sb, N, Sr, Hg, Br C. Sn, N, Ag, Hg, Br N. ne znam (3) 2. Mangan(II)-sulfit ima sledeću hemijsku formulu: A. MnSO 4 D. Mn 2 (SO 3 ) 3 B. Mn(SO 4 ) 2 E. Mn 2 (SO 4 ) 3 C. MnSO 3 N. ne znam (3) 3. Atom sa rednim brojem 28 (Z = 28) i atomskom masom 59 (A r = 59) sadrži: A. 28 neutrona D. 31 neutron B. 31 elektron E. 59 elektrona C. 59 protona N. ne znam (3) 4. Navedene su jednačine koje predstavljaju različite hemijske reakcije. Zaokružite onu koja predstavlja reakciju neutralizacije. A. 3 NO 2 + H 2 O 2 HNO 3 + NO B. N 2 H 4 + O 2 N H 2 O C. Zn(OH) HClO 4 Zn(ClO 4 ) H 2 O D. Ca(H 2 PO 4 ) 2 + H 2 SO 4 CaSO H 3 PO 4 E. Ag + + I AgI N. ne znam (4)
21 ИНФОРМАТОР Oksidacioni brojevi silicijuma, sumpora i barijuma u jonu Si 4 O 11 6 i jedinjenjima H 2 S 2 O 7 i BaO 2 imaju (istim redosledom) sledeće vrednosti: A. II, IV, II D. IV, VI, II B. -VI, VI, II E. III, V, III C. V, III, VII N. ne znam (4) 6. U vodenom rastvoru natrijum-hidroksida dobro se rastvara: A. BaSO 4 D. CaF 2 B. Al(OH) 3 E. PbCrO 4 C. AgBr N. ne znam (5) 7. Koje od navedenih jedinjenja rastvaranjem u vodi daje nitrit-jone? A. KNO 3 D. NaNO 2 B. N 2 O 5 E. NH 4 Cl C. HCN N. ne znam (5) 8. Elektronska konfiguracija titana je: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 2 4s 2. Najviši stepen oksidacije titana u njegovim jedinjenjima je: A. +II D. +VI B. +V E. +VII C. +IV N. ne znam (5) 9. Kada elementarni natrijum reaguje sa vodom nastaju: A. NaH i H 2 D. NaOH i H 2 B. Na 2 O i H 2 O 2 E. Na 2 O 2 i NaH C. nema reakcije N. ne znam (5) 10. Vrednost ph u rastvoru azotne kiseline koncentracije 0,1 mol dm 3 iznosi: A. 0,001 D. 1 B. 3 E. 1 mol dm 3 C N. ne znam (5) 11. Koje od sledećih jedinjenja u vodenom rastvoru pokazuje baznu reakciju? A. H 3 PO 4 D. NaClO 4 B. (NH 4 ) 2 SO 4 E. NH 3 C. KNO 3 N. ne znam (7)
22 50 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 12. Natrijum karbonat ima sledeći sadržaj ugljenika: Podaci: A r (Na) = 23; A r (C) = 12; A r (O) = 16 A. 42,7 % D. 4,8 % B. 11,3 % E. 19,9 % C. 27,5 % N. ne znam (8) 13. Ako 0,44 mol bor oksida potpuno proreaguje sa viškom ugljenika prema reakciji: 2 B 2 O C B 4 C CO koja količina B 4 C 3 nastaje? A. 0,44 mol D. 0,17 mol B. 0,50 mol E. 0,22 mol C. 0,31 mol N. ne znam (8) 14. Treći član jednog homologog niza je jedinjenje sa molekulskom formulom C 3 H 8. Od navedenih formula koja je molekulska formula osmog člana tog niza: A. C 8 H 8 D. C 8 H 16 B. C 8 H 10 E. C 8 H 18 C. C 8 H 14 N. ne znam (3) 15. Koji od navedenih ugljenih hidrata ne redukuje Felingov i Tolensov rastvor: A. saharoza D. fruktoza B. maltoza E. laktoza C. glukoza N. ne znam (4) 16. Dejstvom koncentrovane nitratne kiseline (HONO 2 ) na fenol nastaje: A. 2,4,6-trinitrofenol D. benzen B. benzil-alkohol E. anilin C. nitrobenzen N. ne znam (5) 17. Dejstvom metil-jodida na natrijum-fenolat nastaje: A. dietil-etar D. fenoksibenzen B. dimetil-etar E. metoksibenzen C. dioksan N. ne znam (5)
23 18. Koji od sledećih alkena ima trans-konfiguraciju: ИНФОРМАТОР 51 H 3 C H H CH 2 CH 3 A. C C D. C C H CH 3 H CH 2 CH 3 H H Cl Cl B. C C E. C C H CH 2 CH 3 Cl Cl C. CH 2 =CH 2 N. ne znam (4) 19. Kada se propin uvodi u amonijačni rastvor bakar(i)-hlorida, taloži se: A. Cu C C Cu D. acetilen B. Cu C C CH 3 E. propen C. propan N. ne znam (6) 20. Kada se na brometan u apsolutnom etru deluje opiljcima magnezijuma, a zatim se u reakcionu smešu uvede ugljenik(iv)-oksid, daljom hidrolizom reakcione smeše nastaje jedinjenje A. Redukcijom jedinjenja A sa litijumaluminijumhidridom (LiAlH 4 ) nastaje: A. propen D. propan B. propanska kiselina E. 2-propanol C. 1-propanol N. ne znam (8)
24 52 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ
25 ИНФОРМАТОР 53
26 54 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ
27 ИНФОРМАТОР 55
28 56 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ UNIVERZITET U BEOGRADU 28. jun godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Element čiji je hemijski simbol K spada u: A. prelazne metale D. halogene elemente B. halkogene elemente E. zemnoalkalne metale C. alkalne metale N. ne znam (3) 2. Atom sa atomskim brojem 34 i masenim brojem 79 sadrži: A. 79 elektrona D. 45 protona B. 45 neutrona E. 79 protona C. 34 neutrona N. ne znam (3) 3. Označiti niz u kome su sve supstance sa kovalentnom vezom. A. KCl, O 2, NH 3 D. SO 3, HCN, AgCl B. Fe(NO 3 ) 2, MgSO 4, Na 3 PO 4 E. KBr, AlCl 3, HNO 3 C. CO 2, HBr, C 2 H 4 N. ne znam (3) 4. Maksimalan broj elektrona koji mogu stati na 5d-orbitale iznosi: A. 10 D. 5 B. 14 E. 45 C. 6 N. ne znam (4) 5. U kom od navedenih jedinjenja jod ima oksidacioni broj V? A. HI D. HIO B. KIO 4 E. Na[AgI 2 ] C. KIO 3 N. ne znam (4)
29 ИНФОРМАТОР Koja od navedenih hemijskih reakcija predstavlja reakciju oksido-redukcije? A. HNO 3 + NaOH NaNO 3 + H 2 O D. Pb Cl PbCl 2 B. Zn + 2HCl ZnCl 2 + H 2 E. N 2 O 5 + H 2 O 2HNO 3 C. Ca(HCO 3 ) 2 CaCO 3 + CO 2 + H 2 O N. ne znam (4) 7. Za neku supstancu se kaže da je amfoterna ako: A. se dobro rastvara u vodi D. lako podleže oksidaciji B. je teško isparljiva E. je nestabilna na vazduhu C. reaguje i sa kiselinama i sa bazama N. ne znam (4) 8. Koliko atoma azota se nalazi u 2 mol NH 4 NO 3? A. 2, D. 1, B. 2, E. 8, C. 6, N. ne znam (5) 9. Koje od navedenih jedinjenja u vodenom rastvoru pokazuje baznu reakciju? A. NaCl D. H 2 SO 4 B. K 2 SO 4 E. NaCH 3 COO C. Mg(NO 3 ) 2 N. ne znam (5) 10. U reakciji 5,6 g azota i 9,6 g kiseonika nastaje oksid formule: Podaci: Ar(N) = 14; Ar(O) = 16 A. NO 3 D. N 2 O 3 B. N 2 O E. N 2 O 5 C. NO N. ne znam (7) 11. U rastvoru neke baze koncentracija OH -jona je 0,01 mol/dm 3. Kolika je ph-vrednost ovog rastvora? A. 0,01 D. 14 B. 1 E. 7 C. 12 N. ne znam (7) 12. Masa kalijum-sulfata potrebna za pripremu 250 cm 3 rastvora ove soli koncentracije 0,40 mol/dm 3 je: Podaci: Ar(K) = 39; Ar(O) = 16; Ar(S) = 32 A. 250 g D. 17,4 g B. 4,3 g E. 135 g C. 0,4 g N. ne znam (8)
30 58 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 13. Izračunati masu natrijum-hidroksida koji nastaje u reakciji 234 g natrijum- -peroksida sa vodom prema jednačini: 2Na 2 O 2 (s) + 2H 2 O(l) 4NaOH(aq) + O 2 (g). Podaci: Ar(Na) = 23; Ar(O) = 16; Ar(H) = 1 A. 468 g D. 234 g B. 240 g E. 160 g C. 120 g N. ne znam (8) 14. Jedinjenje čija je strukturna formula OH zove se: CH 3 A. fenol D. toluen B. o-metilfenol E. benzil-alkohol C. m-etilfenol N. ne znam (3) 15. Sledeća reakcija etanoil-hlorida: CH 3 COCl + H 2 O CH 3 COOH + HCl predstavlja reakciju: A. hidrolize D. dehidratacije B. amonolize E. alkoholize C. esterifikacije N. ne znam (4) 16. Oksidacijom propena razblaženim vodenim rastvorom kalijum- -permanganata na sobnoj temperaturi nastaje: A. aceton D. propanska kiselina B. 1,2-propandiol E. propan C. glicerol N. ne znam (5) 17. Koje od navedenih jedinjenja sadrži hiralni ugljenikov atom: A. CH 2 =CHCH 2 CH 3 D. HOOC COOH H B. CH 2 Br E. H 3 C C COOH OH C. CH 3 O CH 3 N. ne znam (4)
31 ИНФОРМАТОР Dejstvom alkil-halogenida na natrijum-alkoksid (alkoholat) nastaje: A. alkohol D. etar B. amid E. karboksilna kiselina C. alkan N. ne znam (5) 19. Zagrevanjem etanske kiseline sa etanolom u prisustvu H + kao katalizatora nastaje: A. etil-etanoat D. etanamid B. etan E. etanoil-hlorid C. metanol N. ne znam (6) 20. Hidratacijom alkena O (C 2 H 4 ) nastaje alkohol P (C 2 H 6 O) koji blagom oksidacijom prelazi u aldehid R (C 2 H 4 O). U slabo baznoj sredini, aldolnom adicijom iz dva molekula aldehida R nastaje aldol S (C 4 H 8 O 2 ). Iz aldola S se zagrevanjem izdvaja molekul vode i nastaje nezasićeni aldehid T (C 4 H 6 O). Jedinjenje T je: A. 2-butanol D. aceton B. butanal E. acetaldehid C. 2-butenal N. ne znam (8) UNIVERZITET U BEOGRADU 28. jun godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. 1. Jedinjenje čija je strukturna formula Broj poena OH zove se: CH 3 A. fenol D. toluen B. o-metilfenol E. benzil-alkohol C. m-etilfenol N. ne znam (3)
32 60 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 2. Sledeća reakcija etanoil-hlorida: CH 3 COCl + H 2 O CH 3 COOH + HCl predstavlja reakciju: A. hidrolize D. dehidratacije B. amonolize E. alkoholize C. esterifikacije N. ne znam (4) 3. Koje od navedenih jedinjenja sadrži hiralni ugljenikov atom: A. CH 2 =CHCH 2 CH 3 D. HOOC COOH H B. CH 2 Br E. H 3 C C COOH OH C. CH 3 O CH 3 N. ne znam (4) 4. Oksidacijom propena razblaženim vodenim rastvorom kalijum- -permanganata na sobnoj temperaturi nastaje: A. aceton D. propanska kiselina B. 1,2-propandiol E. propan C. glicerol N. ne znam (5) 5. Dejstvom alkil-halogenida na natrijum-alkoksid (alkoholat) nastaje: A. alkohol D. etar B. amid E. karboksilna kiselina C. alkan N. ne znam (5) 6. Zagrevanjem etanske kiseline sa etanolom u prisustvu H + kao katalizatora nastaje: A. etil-etanoat D. etanamid B. etan E. etanoil-hlorid C. metanol N. ne znam (6) 7. Hidratacijom alkena O (C 2 H 4 ) nastaje alkohol P (C 2 H 6 O) koji blagom oksidacijom prelazi u aldehid R (C 2 H 4 O). U slabo baznoj sredini, aldolnom adicijom iz dva molekula aldehida R nastaje aldol S (C 4 H 8 O 2 ). Iz aldola S se zagrevanjem izdvaja molekul vode i nastaje nezasićeni aldehid T (C 4 H 6 O). Jedinjenje T je: A. 2-butanol D. aceton B. butanal E. acetaldehid C. 2-butenal N. ne znam (8)
33 ИНФОРМАТОР Element čiji je hemijski simbol K spada u: A. prelazne metale D. halogene elemente B. halkogene elemente E. zemnoalkalne metale C. alkalne metale N. ne znam (3) 9. Atom sa atomskim brojem 34 i masenim brojem 79 sadrži: A. 79 elektrona D. 45 protona B. 45 neutrona E. 79 protona C. 34 neutrona N. ne znam (3) 10. Označiti niz u kome su sve supstance sa kovalentnom vezom. A. KCl, O 2, NH 3 D. SO 3, HCN, AgCl B. Fe(NO 3 ) 2, MgSO 4, Na 3 PO 4 E. KBr, AlCl 3, HNO 3 C. CO 2, HBr, C 2 H 4 N. ne znam (3) 11. Maksimalan broj elektrona koji mogu stati na 5d-orbitale iznosi: A. 10 D. 5 B. 14 E. 45 C. 6 N. ne znam (4) 12. U kom od navedenih jedinjenja jod ima oksidacioni broj V? A. HI D. HIO B. KIO 4 E. Na[AgI 2 ] C. KIO 3 N. ne znam (4) 13. Koja od navedenih hemijskih reakcija predstavlja reakciju oksido-redukcije? A. HNO 3 + NaOH NaNO 3 + H 2 O B. Zn + 2HCl ZnCl 2 + H 2 C. Ca(HCO 3 ) 2 CaCO 3 + CO 2 + H 2 O D. Pb Cl PbCl 2 E. N 2 O 5 + H 2 O 2HNO 3 N. ne znam (4) 14. Za neku supstancu se kaže da je amfoterna ako: A. se dobro rastvara u vodi D. lako podleže oksidaciji B. je teško isparljiva E. je nestabilna na vazduhu C. reaguje i sa kiselinama i sa bazama N. ne znam (4)
34 62 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 15. Koliko atoma azota se nalazi u 2 mol NH 4 NO 3? A. 2, D. 1, B. 2, E. 8, C. 6, N. ne znam (5) 16. Koje od navedenih jedinjenja u vodenom rastvoru pokazuje baznu reakciju? A. NaCl D. H 2 SO 4 B. K 2 SO 4 E. NaCH 3 COO C. Mg(NO 3 ) 2 N. ne znam (5) 17. U reakciji 5,6 g azota i 9,6 g kiseonika nastaje oksid formule: Podaci: Ar(N) = 14; Ar(O) = 16 A. NO 3 D. N 2 O 3 B. N 2 O E. N 2 O 5 C. NO N. ne znam (7) 18. U rastvoru neke baze koncentracija OH -jona je 0,01 mol/dm 3. Kolika je ph-vrednost ovog rastvora? A. 0,01 D. 14 B. 1 E. 7 C. 12 N. ne znam (7) 19. Masa kalijum-sulfata potrebna za pripremu 250 cm 3 rastvora ove soli koncentracije 0,40 mol/dm 3 je: Podaci: Ar(K) = 39; Ar(O) = 16; Ar(S) = 32 A. 250 g D. 17,4 g B. 4,3 g E. 135 g C. 0,4 g N. ne znam (8) 20. Izračunati masu natrijum-hidroksida koji nastaje u reakciji 234 g natrijum- -peroksida sa vodom prema jednačini: 2Na 2 O 2 (s) + 2H 2 O(l) 4NaOH(aq) + O 2 (g). Podaci: Ar(Na) = 23; Ar(O) = 16; Ar(H) = 1 A. 468 g D. 234 g B. 240 g E. 160 g C. 120 g N. ne znam (8)
35 ИНФОРМАТОР 63 UNIVERZITET U BEOGRADU 06. septembar godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Srebro-sulfid ima sledeću hemijsku formulu: A. Ag 2 SO 4 D. Ag 2 S B. AgSO 4 E. AgS 2 C. Ag 2 SO 3 N. ne znam (3) 2. Baza je prema Protolitičkoj teoriji kiselina i baza supstanca koja: A. prima hidroksid-jon D. daje hidroksid-jon B. daje proton E. disosuje C. prima proton N. ne znam (3) 3. Niz sledećih hemijskih elemenata: kadmijum, fosfor, brom, natrijum i azot predstavljen je hemijskim simbolima A. Cd, P, Br, Na, N D. Kr, Fe, Br, Ni, N B. K, F, B, N, As E. Cd, F, B, Na, Au C. Ca, Fe, Ba, Na, N N. ne znam (3) 4. Koja od navedenih supstanci se nalazi u gasovitom stanju na sobnoj temperaturi i standardnom pritisku? A. Al D. NaCl B. H 2 O E. KOH C. O 2 N. ne znam (3) 5. U kom od navedenih jedinjenja mangan ima oksidacioni broj VII? A. MnCl 2 D. K 2 MnO 4 B. KMnO 4 E. MnSO 4 C. MnO 2 N. ne znam (4) 6. Koja od navedenih hemijskih reakcija predstavlja reakciju neutralizacije? A. NH 4 Cl NH 3 + HCl B. Mg + 2HCl MgCl 2 + H 2 C. Zn(OH) 2 + 2HCl ZnCl 2 + 2H 2 O D. AgNO 3 + HCl AgCl + NaNO 3 E. MnO 2 + 4HCl Cl 2 + MnCl 2 + 2H 2 O N. ne znam (4)
36 64 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 7. Koje od navedenih jedinjenja rastvaranjem u vodi daje hipohlorit-jone? A. KClO 4 D. KClO B. KCl E. KClO 3 C. CaCl 2 N. ne znam (5) 8. Deuterijum je: A. alotropska modifikacija vodonika D. halogeni element B. jedinjenje kiseonika i vodonika E. izotop vodonika C. izotop kiseonika N. ne znam (5) 9. Označiti jedinjenje koje se ponaša kao redukciono sredstvo u reakciji predstavljenoj sledećom jednačinom: Na 2 S 2 O 3 + 4Cl 2 + 5H 2 O 8HCl + Na 2 SO 4 + H 2 SO 4. A. Cl 2 D. HCl B. Na 2 S 2 O 3 E. Na 2 SO 4 C. H 2 O N. ne znam (5) 10. Sadržaj aluminijuma u aluminijum-sulfatu iznosi: Podaci: A r (Al) = 27; A r (O) = 16; A r (S) = 32. A. 22 mas.% D. 8 mas.% B. 33 mas.% E. 16 mas.% C. 10 mas.% N. ne znam (7) 11. Rastvor kalijum-hlorida zapremine 24 cm 3 i koncentracije 2,0 mol/dm 3 razblažen je vodom tako da je ukupna zapremina novog rastvora iznosila 160 cm 3. Izračunati koncentraciju soli u novom rastvoru. A. 1,6 mol/dm 3 D. 2,4 mol/dm 3 B. 3,0 mol/dm 3 E. 0,24 mol/dm 3 C. 0,3 mol/dm 3 N. ne znam (7) 12. Izračunati minimalnu zapreminu rastvora kalijum-hidroksida koncentracije 1,4 mol/dm 3 potrebnu za potpunu neutralizaciju 35 cm 3 rastvora sumporne kiseline koncentracije 1,2 mol/dm 3. A. 35 cm 3 D. 12 cm 3 B. 60 cm 3 E. 30 cm 3 C. 14 cm 3 N. ne znam (8) 13. Pri žarenju natrijum-hidrogenkarbonata dolazi do sledeće hemijske reakcije: 2NaHCO 3 (s) Na 2 CO 3 (s) + CO 2 (g) + H 2 O(g). Izračunati masu natrijum-karbonata nastalog žarenjem 252 g natrijum- -hidrogenkarbonata. Podaci: A r (Na) = 23; A r (O) = 16; A r (C) = 12; A r (H) = 1. A. 318 g D. 159 g B. 636 g E. 50 g C. 106 g N. ne znam (8)
37 ИНФОРМАТОР Funkcionalna grupa klase organskih jedinjenja koja se nazivaju ketoni je: A. C C D. O H O O B. C E. C H C. O N. ne znam (3) 15. Jedinjenje čije je ime po IUPAC ovoj nomenklaturi metoksibenzen je: A. alkohol D. keton B. aldehid E. anhidrid C. etar N. ne znam (4) 16. Nezasićena masna kiselina sa 18 C atoma i jednom dvostrukom vezom (u položaju 9 10) je: A. oleinska kiselina D. linolenska kiselina B. stearinska kiselina E. palmitinska kiselina C. linolna kiselina N. ne znam (4) 17. Pri zagrevanju etena na povišenom pritisku u prisustvu malih količina peroksida ili tragova kiseonika nastaje: A. etan D. polivinil-hlorid B. etin E. polietilen C. metan N. ne znam (5) 18. Dejstvom acil-halogenida na fenol nastaje: A. alkohol D. estar B. karboksilna kiselina E. amin C. amid N. ne znam (5) 19. U kiseloj sredini u prisustvu živa(ii)-sulfata etin adira vodu i daje adicioni proizvod koji odmah prelazi (izomerizuje se) u: A.etan D. etanol B.etanal E. acetilen C. eten N. ne znam (6) 20. Adicijom gasovitog hlorovodonika na alken O (C 2 H 4 ) nastaje alkil-halogenid P (C 2 H 5 Cl) koji hidrolizom daje alkohol R (C 2 H 6 O). Iz dva molekula alkohola R se dehidratacijom pod kontrolisanim uslovima temperature ( t = 140 C) i u prisustvu sulfatne kiseline dobija: A. butan D. etoksietan B. etil-etanoat E. etanol C. etil-hlorid N. ne znam (8)
38 66 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ UNIVERZITET U BEOGRADU 06. septembar godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Funkcionalna grupa klase organskih jedinjenja koja se nazivaju ketoni je: A. C C D. O H O O B. C E. C H C. O N. ne znam (3) 2. Jedinjenje čije je ime po IUPAC ovoj nomenklaturi metoksibenzen je: A. alkohol D. keton B. aldehid E. anhidrid C. etar N. ne znam (4) 3. Nezasićena masna kiselina sa 18 C atoma i jednom dvostrukom vezom (u položaju 9 10) je: A. oleinska kiselina D. linolenska kiselina B. stearinska kiselina E. palmitinska kiselina C. linolna kiselina N. ne znam (4) 4. Pri zagrevanju etena na povišenom pritisku u prisustvu malih količina peroksida ili tragova kiseonika nastaje: A. etan D. polivinil-hlorid B. etin E. polietilen C. metan N. ne znam (5) 5. Dejstvom acil-halogenida na fenol nastaje: A. alkohol D. estar B. karboksilna kiselina E. amin C. amid N. ne znam (5) 6. U kiseloj sredini u prisustvu živa(ii)-sulfata etin adira vodu i daje adicioni proizvod koji odmah prelazi (izomerizuje se) u: A.etan D. etanol B.etanal E. acetilen C. eten N. ne znam (6)
39 ИНФОРМАТОР Adicijom gasovitog hlorovodonika na alken O (C 2 H 4 ) nastaje alkil-halogenid P (C 2 H 5 Cl) koji hidrolizom daje alkohol R (C 2 H 6 O). Iz dva molekula alkohola R se dehidratacijom pod kontrolisanim uslovima temperature ( t = 140 C) i u prisustvu sulfatne kiseline dobija: A. butan D. etoksietan B. etil-etanoat E. etanol C. etil-hlorid N. ne znam (8) 8. Srebro-sulfid ima sledeću hemijsku formulu: A. Ag 2 SO 4 D. Ag 2 S B. AgSO 4 E. AgS 2 C. Ag 2 SO 3 N. ne znam (3) 9. Baza je prema Protolitičkoj teoriji kiselina i baza supstanca koja: A. prima hidroksid-jon D. daje hidroksid-jon B. daje proton E. disosuje C. prima proton N. ne znam (3) 10. Niz sledećih hemijskih elemenata: kadmijum, fosfor, brom, natrijum i azot predstavljen je hemijskim simbolima A. Cd, P, Br, Na, N D. Kr, Fe, Br, Ni, N B. K, F, B, N, As E. Cd, F, B, Na, Au C. Ca, Fe, Ba, Na, N N. ne znam (3) 11. Koja od navedenih supstanci se nalazi u gasovitom stanju na sobnoj temperaturi i standardnom pritisku? A. Al D. NaCl B. H 2 O E. KOH C. O 2 N. ne znam (3) 12. U kom od navedenih jedinjenja mangan ima oksidacioni broj VII? A. MnCl 2 D. K 2 MnO 4 B. KMnO 4 E. MnSO 4 C. MnO 2 N. ne znam (4) 13. Koja od navedenih hemijskih reakcija predstavlja reakciju neutralizacije? A. NH 4 Cl NH 3 + HCl B. Mg + 2HCl MgCl 2 + H 2 C. Zn(OH) 2 + 2HCl ZnCl 2 + 2H 2 O D. AgNO 3 + HCl AgCl + NaNO 3 E. MnO 2 + 4HCl Cl 2 + MnCl 2 + 2H 2 O N. ne znam (4) 14. Koje od navedenih jedinjenja rastvaranjem u vodi daje hipohlorit-jone? A. KClO 4 D. KClO B. KCl E. KClO 3 C. CaCl 2 N. ne znam (5)
40 68 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 15. Deuterijum je: A. alotropska modifikacija vodonika D. halogeni element B. jedinjenje kiseonika i vodonika E. izotop vodonika C. izotop kiseonika N. ne znam (5) 16. Označiti jedinjenje koje se ponaša kao redukciono sredstvo u reakciji predstavljenoj sledećom jednačinom: Na 2 S 2 O 3 + 4Cl 2 + 5H 2 O 8HCl + Na 2 SO 4 + H 2 SO 4. A. Cl 2 D. HCl B. Na 2 S 2 O 3 E. Na 2 SO 4 C. H 2 O N. ne znam (5) 17. Sadržaj aluminijuma u aluminijum-sulfatu iznosi: Podaci: A r (Al) = 27; A r (O) = 16; A r (S) = 32. A. 22 mas.% D. 8 mas.% B. 33 mas.% E. 16 mas.% C. 10 mas.% N. ne znam (7) 18. Rastvor kalijum-hlorida zapremine 24 cm 3 i koncentracije 2,0 mol/dm 3 razblažen je vodom tako da je ukupna zapremina novog rastvora iznosila 160 cm 3. Izračunati koncentraciju soli u novom rastvoru. A. 1,6 mol/dm 3 D. 2,4 mol/dm 3 B. 3,0 mol/dm 3 E. 0,24 mol/dm 3 C. 0,3 mol/dm 3 N. ne znam (7) 19. Izračunati minimalnu zapreminu rastvora kalijum-hidroksida koncentracije 1,4 mol/dm 3 potrebnu za potpunu neutralizaciju 35 cm 3 rastvora sumporne kiseline koncentracije 1,2 mol/dm 3. A. 35 cm 3 D. 12 cm 3 B. 60 cm 3 E. 30 cm 3 C. 14 cm 3 N. ne znam (8) 20. Pri žarenju natrijum-hidrogenkarbonata dolazi do sledeće hemijske reakcije: 2NaHCO 3 (s) Na 2 CO 3 (s) + CO 2 (g) + H 2 O(g). Izračunati masu natrijum-karbonata nastalog žarenjem 252 g natrijum- -hidrogenkarbonata. Podaci: A r (Na) = 23; A r (O) = 16; A r (C) = 12; A r (H) = 1. A. 318 g D. 159 g B. 636 g E. 50 g C. 106 g N. ne znam (8)
41 ИНФОРМАТОР 69 UNIVERZITET U BEOGRADU 27. jun godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. 1. Jedinjenje čija je strukturna formula Broj poena OH O zove se: CH A. fenol D. benzaldehid B. o-hidroksibenzaldehid E. formaldehid C. p-hidroksibenzaldehid N. ne znam (3) 2. Sledeća reakcija propanoil-hlorida: CH 3 CH 2 COCl + NH 3 CH 3 CH 2 CONH 2 + HCl predstavlja reakciju: A. amonolize D. alkoholize B. esterifikacije E. hidratacije C. hidrolize N. ne znam (4) 3. Ugljenikovi atomi u prstenu nitrobenzena su: A. sp 2 -hibridizovani D. nisu hibridizovani B. sp-hibridizovani E. mešovito hibridizovani C. sp 3 -hibridizovani N. ne znam (4) 4. Polimerizacijom vinil-hlorida (hloretena) nastaje: A. acetilen D. polietilen B. etilen E. polivinil-hlorid C. propen N. ne znam (5)
42 70 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 5. Kada se 1,2-dibrometan zagreva u alkoholnom rastvoru kalijum-hidroksida nastaje: A. etan D. etanol B. eten E. sirćetna kiselina C. acetilen N. ne znam (5) 6. Dejstvom etil-bromida na natrijum-etoksid nastaje: A. etanol D. metoksietan B. acetamid E. dietil-etar C. etan N. ne znam (6) 7. Na 5,6 g alkena P adira se 16 g broma. Katalitičkom hidrogenizacijom alkena P nastaje zasićeni ugljovodonik R, koji u svom molekulu nema sekundarnih C- atoma. Alken P je: Podaci: A r (Br) = 80; A r (C) = 12; A r (H) = 1 A. 2-metilpropen D. 2,3-dimetil-1-buten B. 2-buten E. 2-metilpropan C. 1-buten N. ne znam (8) 8. Ako jon cinka sadrži 30 protona, 35 neutrona i 28 elektrona njegov simbol je: A. 63 Zn 2+ D. 65 Zn 2+ B. 65 Zn 2 E. 63 Zn 2 C. 35 Zn 2+ N. ne znam (4) 9. Hemijska formula amonijum-sulfida je: A. (NH 3 ) 2 SO 3 D. (NH 4 ) 2 SO 3 B. (NH 4 ) 2 S E. (NH 3 ) 2 S C. (NH 4 ) 2 SO 4 N. ne znam (3) 10. Jednačina C 3 H 8 (g)+ 5O 2 (g) 3CO 2 (g) + 4H 2 O(g) predstavlja reakciju: A. sagorevanja D. jonske izmene B. neutralizacije E. supstitucije C. taloženja N. ne znam (3) 11. Oksidacioni broj sumpora u jedinjenju Na 2 S 2 O 7 je: A. IV D. II B. VI E. 0 C. V N. ne znam (3)
43 ИНФОРМАТОР Označiti niz u kojem su sva jedinjenja sa jonskom vezom. A. H 2 SO 4, NaOH, NaCl D. MgSO 4, NaOH, SO 2 B. ZnCl 2, CO 2, KOH E. MgSO 4, Ca(OH) 2, NaCl C. NH 3, LiOH, NaCl N. ne znam (3) 13. Zaokružiti jedinjenje čiji vodeni rastvor pokazuje kiselu reakciju. A. NaCl D. NH 4 Cl B. NH 3 E. NaNO 3 C. KNO 2 N. ne znam (4) 14. Koji od navedenih oksida pri rastvaranju u vodi gradi kiselinu? A. MgO D. Al 2 O 3 B. Na 2 O E. K 2 O C. N 2 O 5 N. ne znam (5) 15. U reakciji Cu(s) + 4HNO 3 (aq) Cu(NO 3 ) 2 (aq) + 2NO(g) + 2H 2 O(l): A. bakar se oksidovao D. bakar je primio elektrone B. azot se oksidovao E. bakar se redukovao C. azot je otpustio elektrone N. ne znam (5) 16. Reakcija kalijuma sa vodom može se predstaviti sledećom jednačinom: A. 2K(l) + 2H 2 O(l) H 2 (g) + 2KOH(aq) B. 2K(s) + 2H 2 O(l) H 2 (g) + 2KOH(aq) C. 2K(s) + 2H 2 O(l) H 2 (g) + 2KOH(l) D. 2K(s) + 2H 2 O(l) H 2 (l) + 2KOH(aq) E. 2K(l) + 2H 2 O(l) H 2 (l) + 2KOH(s) N. ne znam (5) 17. Ako se u 100 cm 3 vode rastvori 0,05 mol azotne kiseline i 0,06 mol natrijum-hidroksida vrednost ph u dobijenom rastvoru iznosi: A. 1 D. 13 B. 14 E. 12 C. 2 N. ne znam (8) 18. Sadržaj kiseonika u kalcijum-karbonatu iznosi: Podaci: A r (Ca) = 40; A r (C) = 12; A r (O) = 16 A. 40 mas.% D. 16 mas.% B. 32 mas.% E. 48 mas.% C. 64 mas.% N. ne znam (7)
44 72 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 19. Rastvor natrijum-sulfata zapremine 25 cm 3 i koncentracije 0,1 mol/dm 3 razblažen je vodom do zapremine od 100 cm 3. Izračunati koncentraciju soli u novom rastvoru. A. 0,25 mol/dm 3 D. 0,02 mol/dm 3 B. 0,025 mol/dm 3 E. 0,5 mol/dm 3 C. 0,05 mol/dm 3 N. ne znam (7) 20. Izračunati zapreminu rastvora hlorovodonične kiseline koncentracije 2,0 mol/dm 3 koja je potrebna za reakciju sa 32,5 g cinka. Podatak: A r (Zn) = 65 A. 0,5 dm 3 D. 2 dm 3 B. 1 dm 3 E. 1,5 dm 3 C. 0,05 dm 3 N. ne znam (8)
45 ИНФОРМАТОР 73 UNIVERZITET U BEOGRADU 25. jun godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Ako je relativna atomska masa nekog elementa 76, a njegov atom sadrži 33 neutrona, atomski broj elementa (Z) je: A. 33 D. 76 B. 43 E. 40 C. 109 N. ne znam (3) 2. Hemijska formula kalijum-cijanida je: A. K 2 CN D. K 2 SCN B. K(CN) 2 E. KCN C. KSCN N. ne znam (3) 3. Zapremina od 150 ml jednaka je: A. 1,5 l D. 15 cm 3 B. 150 dm 3 E. 0,15 dm 3 C l N. ne znam (3) 4. Koja od navedenih jednačina predstavlja reakciju neutralizacije? A. Ca(NO 3 ) 2 + H 2 SO 4 CaSO 4 + 2HNO 3 B. Ag + + Cl AgCl C. 2NH 3 + H 2 SO 4 (NH 4 ) 2 SO 4 D. 2Na + 2H 2 O 2NaOH + H 2 E. N 2 O 5 + H 2 O 2HNO 3 N. ne znam (5) 5. U jednačini 2H 2 S + SO 2 3S + 2H 2 O oksidacioni brojevi sumpora su redom: A. +II, IV, I D. II, IV, 0 B. II, VI, 0 E. II, IV, I C. +II, VI, 0 N. ne znam (5)
46 74 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 6. Označiti niz u kojem su sva jedinjenja koja grade vodonične veze. A. H 2 O, CH 4, HF D. NH 3, CaO, HNO 3 B. NH 3, H 2 SO 4, MgO E. HF, H 2 O, Na 2 O C. NH 3, H 2 O, HF N. ne znam (3) 7. Hloriti su soli sledeće kiseline: A. HClO D. HClO 4 B. HClO 2 E. HCl C. HClO 3 N. ne znam (4) 8. Ako se u vodi rastvori po 1 mol NaOH i CH 3 COOH dobijeni rastvor reaguje: A. bazno D. amfoterno B. kiselo E. kiselo-bazno C. neutralno N. ne znam (4) 9. Označiti redukciono sredstvo u reakciji 3PbO(s) + 2NH 3 (g) 3Pb(s) + N 2 (g) + 3H 2 O(l). A. PbO D. N 2 B. NH 3 E. H 2 O C. Pb N. ne znam (5) 10. Izračunati masu natrijum-nitrita koju je potrebno rastvoriti u 60 g vode da bi se dobio 20 mas.% rastvor. A. 80 g D. 150 g B. 30 g E. 20 g C. 15 g N. ne znam (7) 11. U jednačini KMnO 4 + KI + H 2 O MnO 2 + I 2 + KOH, stehiometrijski koeficijenti KMnO 4, KI i I 2 su redom: A. 4, 6, 2 D. 2, 6, 3 B. 1, 3, 3 E. 1, 3, 1 C. 2, 6, 4 N. ne znam (7) 12. Izračunati zapreminu rastvora azotne kiseline koncentracije 1,0 mol/dm 3 koja je potrebna za neutralizaciju 20 cm 3 rastvora natrijum-hidroksida koncentracije 1,5 mol/dm 3. A. 30 dm 3 D. 0,30 cm 3 B. 15 cm 3 E. 30 cm 3 C. 0,15 cm 3 N. ne znam (8)
47 ИНФОРМАТОР Izračunati masu kalcijum-karbonata koji nastaje termičkim razlaganjem 324 g kalcijum-hidrogenkarbonata prema jednačini: Ca(HCO 3 ) 2 (s) CaCO 3 (s) + CO 2 (g) + H 2 O(g). Podaci: A r (Ca) = 40; A r (H) = 1; A r (C) = 12; A r (O) = 16. A. 100 g D. 200 g B. 10 g E. 250 g C. 20 g N. ne znam (8) 14. Jedinjenje čija je strukturna formula C OH H 3 zove se: A. fenol D. trotil B. o-metilfenol E. toluen C. m-metilfenol N. ne znam (3) 15. Sledeća reakcija etanoil-hlorida: CH 3 COCl + CH 3 OH CH 3 COOCH 3 + HCl predstavlja reakciju: A. amonolize D. alkoholize B. dekarboksilacije E. hidrolize C. hidratacije N. ne znam (4) 16. Ugljenikovi atomi u molekulu cikloheksana su: A. sp 2 -hibridizovani D. nisu hibridizovani B. sp 3 -hibridizovani E. mešovito hibridizovani C. sp-hibridizovani N. ne znam (4) 17. U benzenu vodonikov atom moguće je supstituisati u prisustvu anhidrovanog AlCl 3 etil-grupom pomoću: A. CH 3 CH 2 Cl D. CH 3 O CH 3 B. CH 3 CH 3 E. H 2 C=O C. CH 3 COOH N. ne znam (5) 18. Elektrofilnom adicijom hlorovodonika na propen nastaje: A. 2,2-dihlorpropan D. vinil-hlorid B. 1-brompropan E. alil-hlorid C. 2-hlorpropan N. ne znam (5)
48 76 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 19. Dejstvom anilina na benzendiazonijum-hlorid nastaje: A. aminokiselina D. nitro-jedinjenje B. amid E. azo-boja C. acetal N. ne znam (6) 20. Kada se na metilmagnezijum-bromid u apsolutnom etru deluje metanalom, daljom hidrolizom reakcione smeše nastaje jedinjenje A. Dejstvom fosfor(v)- hlorida na jedinjenje A nastaje: A. sirćetna kiselina D. acetilen B. etanol E. etanal C. etil-hlorid N. ne znam (8)
49 ИНФОРМАТОР 77 UNIVERZITET U BEOGRADU 01. jul godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Ako se u jezgru nekog atoma nalazi 82 neutrona, a njegov maseni broj je 138, onda jezgro tog atoma sadrži: A. 138 protona D. 82 elektrona B. 82 protona E. 138 elektrona C. 56 protona N. ne znam (3) 2. Natrijum-hidrogenfosfat ima sledeću hemijsku formulu: A. Na 2 H 2 PO 4 D. Na 2 HPO 4 B. Na 3 PO 4 E. Na 3 HPO 4 C. NaH 2 PO 4 N. ne znam (3) 3. Reakcije oksido-redukcije su reakcije u kojima dolazi do: A. promene ph sredine B. prelaska protona sa jedne hemijske vrste na drugu C. promene oksidacionih stanja nekih atoma u jedinjenjima koja reaguju D. oslobađanja velike količine toplote E. izdvajanja gasovitih proizvoda reakcije N. ne znam (3) 4. Ako gasovi N 2 i NO 2 na istom pritisku i temperaturi zauzimaju istu zapreminu onda imaju: A. jednake količine D. jednak broj atoma B. jednaku masu E. jednaku sitšljivost C. jednaku gustinu N. ne znam (4) 5. Koja supstanca rastvaranjem u vodi neće uticati na promenu ph? A. Na 2 S D. K 2 S B. Na 2 SO 4 E. ZnSO 4 C. K 2 SO 3 N. ne znam (4)
50 78 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 6. Oksidacioni brojevi olova, azota i hroma u jedinjenjima PbO 2, (NH 4 ) 2 SO 4, K 2 Cr 2 O 7 imaju (istim redosledom) sledeće vrednosti: A. IV, III, VI D. IV, III, VI B. II, III, III E. IV, III, VI C. II, III, VI N. ne znam (4) 7. Kada aluminijum reaguje sa koncentrovanim rastvorom natrijum-hidroksida nastaje: A. Al(OH) 3 i H 2 D. Al(OH) 3 i H 2 O B. Na[Al(OH) 4 ] i H 2 E. Al 2 O 3 i H 2 O C. Na[Al(OH) 4 ] i H 2 O N. ne znam (5) 8. Koja supstanca se ponaša kao oksidaciono sredstvo u sledećoj reakciji predstavljenoj jednačinom: 2KBr + (NH 4 ) 2 S 2 O 8 Br 2 + K 2 SO 4 + (NH 4 ) 2 SO 4? A. KBr D. K 2 SO 4 B. (NH 4 ) 2 S 2 O 8 E. (NH 4 ) 2 SO 4 C. Br 2 N. ne znam (5) 9. U rastvoru kalijum-hidroksida koncentracije 0,001 mol/dm 3 ph-vrednost iznosi: A. 3 D. 11 B. 1 E. 7 C. 14 N. ne znam (4) 10. Izračunati broj molekula koji se nalazi u 507,6 g elementarnog joda. Podaci: A r (I) = 126,9 A. 1, D. 1, B. 4, E. 2, C. 6, N. ne znam (7) 11. Kolika masa kalcijum-hlorida je potrebna za pripremu 200 cm 3 rastvora ove soli koncentracije 0,50 mol/dm 3? Podaci: A r (Ca) = 40; A r (Cl) = 35,5 A. 7,55 g D. 75,5 g B. 15,1 g E. 11,1 g C. 1,11 g N. ne znam (7)
51 ИНФОРМАТОР Procentni sastav (mas.%) bakar(ii)-nitrata je: Podaci: A r (Cu) = 63,5; A r (N) = 14; A r (O) = 16 A. 53,5 % Cu; 16,8 % N; 29,7 % O B. 38,2 % Cu; 18,3 % N; 43,5 % O C. 33,9 % Cu; 14,9 % N; 51,2 % O D. 50,6 % Cu; 11,2 % N; 38,2 % O E. 45,7 % Cu; 33,6 % N; 20,7 % O N. ne znam (8) 13. Izračunati masu gvožđa koje nastaje kada 798 kg gvožđe(iii)-oksida proreaguje sa viškom ugljen-monoksida u reakciji predstavljenoj jednačinom: Fe 2 O 3 (s) + 3CO(g) 2Fe(s) + 3CO 2 (g). Podaci: A r (Fe) = 55,8; A r (O) = 16 A. 279 kg D. 372 kg B. 55,8 kg E. 558 kg C. 2,79 kg N. ne znam (8) 14. Koja od navedenih formula je tačna formula ugljovodonika: A. CH 2 =CH 2 CH 2 CH 3 D. CH 3 CH 2 CH=CH 2 B. CH 2 =CH CH CH 3 E. CH 3 CH(CH 3 ) 2 CH 3 C. CH 3 CH 2 =CH CH 3 N. ne znam (3) 15. Sledeća reakcija 2-butenala CH 3 CH CHCHO + 2 H 2 Ni predstavlja reakciju: CH 3 CH 2 CH 2 CH 2 OH A. hidrogenizacije D. dehidratacije B. hidratacije E. alkoholize C. oksidacije N. ne znam (4) 16. Hejvortova perspektivna formula HOH 2 C OH O HO predstavlja: CH 2 OH OH A. β-d-glukopiranozu D. α-d-fruktofuranozu B. β-d-glukofuranozu E. β-d-fruktofuranozu C. α-d-glukofuranozu N. ne znam (4)
52 80 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 17. Dietil-etar sa koncentrovanom hloridnom kiselinom (HCl) gradi: A. oksonijum-so D. aldol B. karboksilnu kiselinu E. alkan C. alkohol N. ne znam (5) 18. Dejstvom acil-halogenida na fenol nastaje: A. merkaptan D. anhidrid B. estar E. etar C. amid N. ne znam (5) 19. Redukcijom etanamida sa litijum-aluminijumhidridom (LiAlH 4 ) nastaje: A. etan D. karbamid B. sirćetna kiselina E. etilamin C. nitrometan N. ne znam (6) 20. Kada se na jodmetan u apsolutnom etru deluje opiljcima magnezijuma, a zatim se u reakcionu smešu uvede ugljenik(iv)-oksid, daljom hidrolizom reakcione smeše nastaje jedinjenje A. Zagrevanjem jedinjenja A sa etanolom, u prisustvu H + kao katalizatora, nastaje: A. etanamid D. etil-etanoat B. sirćetna kiselina E. etanoil-hlorid C. metanol N. ne znam (8)
53 ИНФОРМАТОР 81 UNIVERZITET U BEOGRADU 01. jul godine KLASIFIKACIONI ISPIT IZ HEMIJE ZA UPIS NA TEHNOLOŠKO-METALURŠKI FAKULTET U BEOGRADU Šifra zadatka: Test ima 20 pitanja. Netačan odgovor donosi 10% od broja poena za tačan zadatak. Zaokruživanje više od jednog odgovora, kao i nezaokruživanje nijednog odgovora donosi 1 poen. Broj poena 1. Koja od navedenih formula je tačna formula ugljovodonika: A. CH 2 =CH 2 CH 2 CH 3 D. CH 3 CH 2 CH=CH 2 B. CH 2 =CH CH CH 3 E. CH 3 CH(CH 3 ) 2 CH 3 C. CH 3 CH 2 =CH CH 3 N. ne znam (3) 2. Sledeća reakcija 2-butenala CH 3 CH CHCHO + 2 H 2 Ni predstavlja reakciju: CH 3 CH 2 CH 2 CH 2 OH A. hidrogenizacije D. dehidratacije B. hidratacije E. alkoholize C. oksidacije N. ne znam (4) 3. Hejvortova perspektivna formula HOH 2 C OH O HO predstavlja: CH 2 OH OH A. β-d-glukopiranozu D. α-d-fruktofuranozu B. β-d-glukofuranozu E. β-d-fruktofuranozu C. α-d-glukofuranozu N. ne znam (4) 4. Dietil-etar sa koncentrovanom hloridnom kiselinom (HCl) gradi: A. oksonijum-so D. aldol B. karboksilnu kiselinu E. alkan C. alkohol N. ne znam (5)
54 82 ТЕХНОЛОШКО-МЕТАЛУРШКИ ФАКУЛТЕТ 5. Dejstvom acil-halogenida na fenol nastaje: A. merkaptan D. anhidrid B. estar E. etar C. amid N. ne znam (5) 6. Redukcijom etanamida sa litijum-aluminijumhidridom (LiAlH 4 ) nastaje: A. etan D. karbamid B. sirćetna kiselina E. etilamin C. nitrometan N. ne znam (6) 7. Kada se na jodmetan u apsolutnom etru deluje opiljcima magnezijuma, a zatim se u reakcionu smešu uvede ugljenik(iv)-oksid, daljom hidrolizom reakcione smeše nastaje jedinjenje A. Zagrevanjem jedinjenja A sa etanolom, u prisustvu H + kao katalizatora, nastaje: A. etanamid D. etil-etanoat B. sirćetna kiselina E. etanoil-hlorid C. metanol N. ne znam (8) 8. Ako se u jezgru nekog atoma nalazi 82 neutrona, a njegov maseni broj je 138, onda jezgro tog atoma sadrži: A. 138 protona D. 82 elektrona B. 82 protona E. 138 elektrona C. 56 protona N. ne znam (3) 9. Reakcije oksido-redukcije su reakcije u kojima dolazi do: A. promene ph sredine B. prelaska protona sa jedne hemijske vrste na drugu C. promene oksidacionih stanja nekih atoma u jedinjenjima koja reaguju D. oslobađanja velike količine toplote E. izdvajanja gasovitih proizvoda reakcije N. ne znam (3) 10. Natrijum-hidrogenfosfat ima sledeću hemijsku formulu: A. Na 2 H 2 PO 4 D. Na 2 HPO 4 B. Na 3 PO 4 E. Na 3 HPO 4 C. NaH 2 PO 4 N. ne znam (3) 11. Ako gasovi N 2 i NO 2 na istom pritisku i temperaturi zauzimaju istu zapreminu onda imaju: A. jednake količine D. jednak broj atoma B. jednaku masu E. jednaku sitšljivost C. jednaku gustinu N. ne znam (4)
55 ИНФОРМАТОР Koja supstanca rastvaranjem u vodi neće uticati na promenu ph? A. Na 2 S D. K 2 S B. Na 2 SO 4 E. ZnSO 4 C. K 2 SO 3 N. ne znam (4) 13. Oksidacioni brojevi olova, azota i hroma u jedinjenjima PbO 2, (NH 4 ) 2 SO 4, K 2 Cr 2 O 7 imaju (istim redosledom) sledeće vrednosti: A. IV, III, VI D. IV, III, VI B. II, III, III E. IV, III, VI C. II, III, VI N. ne znam (4) 14. Kada aluminijum reaguje sa koncentrovanim rastvorom natrijum-hidroksida nastaje: A. Al(OH) 3 i H 2 D. Al(OH) 3 i H 2 O B. Na[Al(OH) 4 ] i H 2 E. Al 2 O 3 i H 2 O C. Na[Al(OH) 4 ] i H 2 O N. ne znam (5) 15. Koja supstanca se ponaša kao oksidaciono sredstvo u sledećoj reakciji predstavljenoj jednačinom: 2KBr + (NH 4 ) 2 S 2 O 8 Br 2 + K 2 SO 4 + (NH 4 ) 2 SO 4? A. KBr D. K 2 SO 4 B. (NH 4 ) 2 S 2 O 8 E. (NH 4 ) 2 SO 4 C. Br 2 N. ne znam (5) 16. U rastvoru kalijum-hidroksida koncentracije 0,001 mol/dm 3 ph-vrednost iznosi: A. 3 D. 11 B. 1 E. 7 C. 14 N. ne znam (4) 17. Izračunati broj molekula koji se nalazi u 507,6 g elementarnog joda. Podaci: A r (I) = 126,9 A. 1, D. 1, B. 4, E. 2, C. 6, N. ne znam (7) 18. Kolika masa kalcijum-hlorida je potrebna za pripremu 200 cm 3 rastvora ove soli koncentracije 0,50 mol/dm 3? Podaci: A r (Ca) = 40; A r (Cl) = 35,5 A. 7,55 g D. 75,5 g B. 15,1 g E. 11,1 g C. 1,11 g N. ne znam (7)
Microsoft Word - Test 2009 I.doc
 Ime i prezime (ŠTAMPANIM SLOVIMA!!!) jedinstveni matični broj građana (prepisati iz lične karte) broj prijave Test za prijemni ispit iz hemije 1. Hemijska promena je: a) rastvaranje NaCl b) sublimacija
Ime i prezime (ŠTAMPANIM SLOVIMA!!!) jedinstveni matični broj građana (prepisati iz lične karte) broj prijave Test za prijemni ispit iz hemije 1. Hemijska promena je: a) rastvaranje NaCl b) sublimacija
Zadaci
 Hemijski fakultet Univerziteta u Beogradu Prijemni ispit, 30. jun 2013. godine Test iz hemije Ime i prezime:. Redni broj prijave:. Napomena: Test raditi isključivo plavom ili crnom hemijskom olovkom. Vreme
Hemijski fakultet Univerziteta u Beogradu Prijemni ispit, 30. jun 2013. godine Test iz hemije Ime i prezime:. Redni broj prijave:. Napomena: Test raditi isključivo plavom ili crnom hemijskom olovkom. Vreme
Univerzitet u Nišu Prirodno-matematički fakultet Departman za hemiju Prijemni ispit za upis na Osnovne akademske studije hemije na PMF-u u Nišu školsk
 Univerzitet u Nišu Prirodno-matematički fakultet Departman za hemiju Prijemni ispit za upis na Osnovne akademske studije hemije na PMF-u u Nišu školske 2019/20. godine Test se popunjava zaokruživanjem
Univerzitet u Nišu Prirodno-matematički fakultet Departman za hemiju Prijemni ispit za upis na Osnovne akademske studije hemije na PMF-u u Nišu školske 2019/20. godine Test se popunjava zaokruživanjem
Министарство просвете, науке и технолошког развоја ОКРУЖНО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ 22. април године ТЕСТ ЗА 8. РАЗРЕД Шифра ученика Српско хемијско
 Министарство просвете, науке и технолошког развоја ОКРУЖНО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ 22. април 2018. године ТЕСТ ЗА 8. РАЗРЕД Шифра ученика Српско хемијско друштво (три слова и три броја) УПИШИ Х ПОРЕД НАВЕДЕНЕ
Министарство просвете, науке и технолошког развоја ОКРУЖНО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ 22. април 2018. године ТЕСТ ЗА 8. РАЗРЕД Шифра ученика Српско хемијско друштво (три слова и три броја) УПИШИ Х ПОРЕД НАВЕДЕНЕ
Министарство просветe и спортa Републике Србије
 Министарство просветe и спортa Републике Србије Српско хемијско друштво Републичко такмичење из хемије 21.05.2005. Тест за I разред средње школе Име и презиме Место и школа Разред Не отварајте добијени
Министарство просветe и спортa Републике Србије Српско хемијско друштво Републичко такмичење из хемије 21.05.2005. Тест за I разред средње школе Име и презиме Место и школа Разред Не отварајте добијени
РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕПУБЛИЧКО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ Лесковац, 31. мај и 1. јун
 РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕПУБЛИЧКО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ Лесковац, 31. мај и 1. јун 2014. године ТЕСТ ЗНАЊА ЗА VIII РАЗРЕД Шифра ученика
РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕПУБЛИЧКО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ Лесковац, 31. мај и 1. јун 2014. године ТЕСТ ЗНАЊА ЗА VIII РАЗРЕД Шифра ученика
Савез хемичара и технолога Македоније Такмичења из хемије за ученике основних и средњих школа ШИФРА: (уноси комисија по завршетку тестирања овде и на
 Савез хемичара и технолога Македоније Такмичења из хемије за ученике основних и средњих школа ШИФРА: (уноси комисија по завршетку тестирања овде и на коверту) ОКРУЖНО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ 6 април, 2019
Савез хемичара и технолога Македоније Такмичења из хемије за ученике основних и средњих школа ШИФРА: (уноси комисија по завршетку тестирања овде и на коверту) ОКРУЖНО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ 6 април, 2019
РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕПУБЛИЧКО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ Лесковац, 31. мај и 1. јун
 РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕПУБЛИЧКО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ Лесковац, 31. мај и 1. јун 2014. године ТЕСТ ЗНАЊА ЗА VII РАЗРЕД Шифра ученика
РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕПУБЛИЧКО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ Лесковац, 31. мај и 1. јун 2014. године ТЕСТ ЗНАЊА ЗА VII РАЗРЕД Шифра ученика
Regionalno_test_VIII_2013_hemija
 РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕГИОНАЛНО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ (7. април 2013. године) ТЕСТ ЗНАЊА ЗА VIII РАЗРЕД Шифра ученика: Пажљиво прочитај
РЕПУБЛИКА СРБИЈА МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА СРПСКО ХЕМИЈСКО ДРУШТВО РЕГИОНАЛНО ТАКМИЧЕЊЕ ИЗ ХЕМИЈЕ (7. април 2013. године) ТЕСТ ЗНАЊА ЗА VIII РАЗРЕД Шифра ученика: Пажљиво прочитај
Uputstva za takmičare: Zadatak (broj) Ukupan broj bodova na testu: 100 Bodovi
 Uputstva za takmičare: Zadatak (broj) Ukupan broj bodova na testu: 100 Bodovi 1. 6. 4. 5 4. 8 5. 8 6. 7. 8 8. 4 9. 5 10. 8 11. 1. 1. 14. 15. 5 16. 4 17. 5 18. 5 19. 6 0. 4 1.. Za izradu testa planirano
Uputstva za takmičare: Zadatak (broj) Ukupan broj bodova na testu: 100 Bodovi 1. 6. 4. 5 4. 8 5. 8 6. 7. 8 8. 4 9. 5 10. 8 11. 1. 1. 14. 15. 5 16. 4 17. 5 18. 5 19. 6 0. 4 1.. Za izradu testa planirano
МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА РЕПУБЛИКЕ СРБИЈЕ ЗАВОД ЗА УНАПРЕЂИВАЊE ОБРАЗОВАЊА И ВАСПИТАЊА Пословно удружење средњих стручних шк
 МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА РЕПУБЛИКЕ СРБИЈЕ ЗАВОД ЗА УНАПРЕЂИВАЊE ОБРАЗОВАЊА И ВАСПИТАЊА Пословно удружење средњих стручних школа Републике Србије за подручје рада Хемија, неметали
МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА РЕПУБЛИКЕ СРБИЈЕ ЗАВОД ЗА УНАПРЕЂИВАЊE ОБРАЗОВАЊА И ВАСПИТАЊА Пословно удружење средњих стручних школа Републике Србије за подручје рада Хемија, неметали
ZADACI_KEMIJA_2008_1_A
 RAZREDBENI ISPIT 2008. (GRUPA A) ŠIFRA: Rješenje svakog zadatka treba označiti u Tablici s rješenjima znakom «X». U svakom zadatku samo je jedan predloženi odgovor točan. Svaki točno riješeni zadatak donosi
RAZREDBENI ISPIT 2008. (GRUPA A) ŠIFRA: Rješenje svakog zadatka treba označiti u Tablici s rješenjima znakom «X». U svakom zadatku samo je jedan predloženi odgovor točan. Svaki točno riješeni zadatak donosi
Министарство просветe и науке Републике Србије
 Министарство просветe и науке Републике Србије Српско хемијско друштво Републичко такмичење из хемије Ниш, 21.05.2011. Тест за I разред средње школе Име и презиме Место и школа Разред Не отварајте добијени
Министарство просветe и науке Републике Србије Српско хемијско друштво Републичко такмичење из хемије Ниш, 21.05.2011. Тест за I разред средње школе Име и презиме Место и школа Разред Не отварајте добијени
Alkeni nastavak
 Alkeni nastavak 2. Dehidratacija alkohola U industriji: prevođenjem alkoholnih para preko Al 2 O 3 (Lewis-ova kiselina). Laboratorijsko dobijanje Akohol može biti: 3, 2 ili 1. THF tetrahidrofuran -rastvarač
Alkeni nastavak 2. Dehidratacija alkohola U industriji: prevođenjem alkoholnih para preko Al 2 O 3 (Lewis-ova kiselina). Laboratorijsko dobijanje Akohol može biti: 3, 2 ili 1. THF tetrahidrofuran -rastvarač
Министарство просветe и науке Републике Србије
 Министарство просветe и науке Републике Србије Српско хемијско друштво Републичко такмичење из хемије Ниш, 21.05.2011. Тест за II разред средње школе Име и презиме Место и школа Разред Не отварајте добијени
Министарство просветe и науке Републике Србије Српско хемијско друштво Републичко такмичење из хемије Ниш, 21.05.2011. Тест за II разред средње школе Име и презиме Место и школа Разред Не отварајте добијени
Microsoft PowerPoint - 08_Halogeni elementi [Compatibility Mode]
![Microsoft PowerPoint - 08_Halogeni elementi [Compatibility Mode] Microsoft PowerPoint - 08_Halogeni elementi [Compatibility Mode]](/thumbs/102/153188708.jpg) 17. grupa Periodnog sistema elemenata. Zajednički simbol X. Ne nalaze se u prirodi u elementarnom stanju (zbog velike reaktivnosti), već u obliku: F minerala fluorita (CaF 2 ) Cl minerala halita (NaCl)
17. grupa Periodnog sistema elemenata. Zajednički simbol X. Ne nalaze se u prirodi u elementarnom stanju (zbog velike reaktivnosti), već u obliku: F minerala fluorita (CaF 2 ) Cl minerala halita (NaCl)
Хемијски састав ћелије *Подсетник Хемијски елемент је супстанца која се, хемијском реакцијом, не може претворити удругу супстанцу. Најмањи део хемијск
 Хемијски састав ћелије *Подсетник Хемијски елемент је супстанца која се, хемијском реакцијом, не може претворити удругу супстанцу. Најмањи део хемијског елемента који задржава његове особине је атом. Хемијско
Хемијски састав ћелије *Подсетник Хемијски елемент је супстанца која се, хемијском реакцијом, не може претворити удругу супстанцу. Најмањи део хемијског елемента који задржава његове особине је атом. Хемијско
MergedFile
 27. јун 2019. Тест из ХЕМИЈЕ Група: A Тест из ХЕМИЈЕ има 15 питања на 4 стране. Сва питања вреде по 2 поена. Нема негативних поена. NA = 6 10 23 mol -1 ; Vm = 22,4 dm 3 mol -1 ; Ar: H-1; Na-23; O-16; S-32;
27. јун 2019. Тест из ХЕМИЈЕ Група: A Тест из ХЕМИЈЕ има 15 питања на 4 стране. Сва питања вреде по 2 поена. Нема негативних поена. NA = 6 10 23 mol -1 ; Vm = 22,4 dm 3 mol -1 ; Ar: H-1; Na-23; O-16; S-32;
Chapter 23
 Poglavlje 23: Estarski enolati i Claisen-ova kondenzacija Podsećanje: aldolna kondenzacija Claisen-ova kondenzacija Kiseo proton Mehanizam: Adicija-eliminacija 1. korak: formiranje estarskog enolata Alkoksid
Poglavlje 23: Estarski enolati i Claisen-ova kondenzacija Podsećanje: aldolna kondenzacija Claisen-ova kondenzacija Kiseo proton Mehanizam: Adicija-eliminacija 1. korak: formiranje estarskog enolata Alkoksid
ФАКУЛТЕТ ТЕХНИЧКИХ НАУКА ОДСЕК ЗА ПРОИЗВОДНО МАШИНСТВО ПРОЈЕКТОВАЊЕ ТЕХНОЛОГИЈЕ ТЕРМИЧКЕ ОБРАДЕ ХЕМИЈСКО ДЕЈСТВО ОКОЛИНЕ У ПРОЦЕСИМА ТЕРМИЧКЕ ОБРАДЕ -
 ФАКУЛТЕТ ТЕХНИЧКИХ НАУКА ОДСЕК ЗА ПРОИЗВОДНО МАШИНСТВО ПРОЈЕКТОВАЊЕ ТЕХНОЛОГИЈЕ ТЕРМИЧКЕ ОБРАДЕ ХЕМИЈСКО ДЕЈСТВО ОКОЛИНЕ У ПРОЦЕСИМА ТЕРМИЧКЕ ОБРАДЕ - РАДНО - ПРИРЕДИО: ДОЦ. ДР АЛЕКСАНДАР МИЛЕТИЋ SADRŽAJ
ФАКУЛТЕТ ТЕХНИЧКИХ НАУКА ОДСЕК ЗА ПРОИЗВОДНО МАШИНСТВО ПРОЈЕКТОВАЊЕ ТЕХНОЛОГИЈЕ ТЕРМИЧКЕ ОБРАДЕ ХЕМИЈСКО ДЕЈСТВО ОКОЛИНЕ У ПРОЦЕСИМА ТЕРМИЧКЕ ОБРАДЕ - РАДНО - ПРИРЕДИО: ДОЦ. ДР АЛЕКСАНДАР МИЛЕТИЋ SADRŽAJ
PowerPoint Presentation
 ŠTA JE TO ORGANSKA HEMIJA I ZAŠTO JE PROUČAVAMO? ORGANSKO-PRIRODNO- HEMIJSKO-HEMIKALIJA? Organska hemija ili Svijet karbona Organske supstance (npr. maslinovo ulje, šećer, škrob, svila, guma, papir, penicilin
ŠTA JE TO ORGANSKA HEMIJA I ZAŠTO JE PROUČAVAMO? ORGANSKO-PRIRODNO- HEMIJSKO-HEMIKALIJA? Organska hemija ili Svijet karbona Organske supstance (npr. maslinovo ulje, šećer, škrob, svila, guma, papir, penicilin
KATALOG PITANJA IZ HEMIJE ZA OSNOVNE ŠKOLE
 2018. KATALOG PITANJA IZ HEMIJE ZA OSNOVNE ŠKOLE PEDAGOŠKI ZAVOD TUZLANSKOG KANTONA TUZLA 1 BOSNA I HERCEGOVINA FEDERACIJA BOSNE I HERCEGOVINE TUZLANSKI KANTON PEDAGOŠKI ZAVOD TUZLANSKOG KANTONA - TUZLA
2018. KATALOG PITANJA IZ HEMIJE ZA OSNOVNE ŠKOLE PEDAGOŠKI ZAVOD TUZLANSKOG KANTONA TUZLA 1 BOSNA I HERCEGOVINA FEDERACIJA BOSNE I HERCEGOVINE TUZLANSKI KANTON PEDAGOŠKI ZAVOD TUZLANSKOG KANTONA - TUZLA
Kvalitet voda 2012
 Назив реке - ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА Шифра станице - 7805 7805 7805 7805 7805 7805 7805 7805 7805 7805 7805 7805 Ознака места узорковања - A1
Назив реке - ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА ЂЕТИЊА Шифра станице - 7805 7805 7805 7805 7805 7805 7805 7805 7805 7805 7805 7805 Ознака места узорковања - A1
Microsoft Word - Vježba 5.
 5. MASTI I ULJA Pokus 1. ODREĐIVANJE JODNOG BROJA MASLINOVOG I SUNCOKRETOVOG ULJA Jodni broj izražava u postotcima onu količinu joda koju može vezati adicijom neka mast (ulje) ili masna kiselina. Nezasićene
5. MASTI I ULJA Pokus 1. ODREĐIVANJE JODNOG BROJA MASLINOVOG I SUNCOKRETOVOG ULJA Jodni broj izražava u postotcima onu količinu joda koju može vezati adicijom neka mast (ulje) ili masna kiselina. Nezasićene
Primena instrumentalnih metoda na analizu uzoraka vode Zoran Simi ć, master inženjer tehnologije Tehnološko-metalurški fakultet Univerziteta u Beograd
 Primena instrumentalnih metoda na analizu uzoraka vode Zoran Simi ć, master inženjer tehnologije Tehnološko-metalurški fakultet Univerziteta u Beogradu, Beograd 1 Uredba o granicnim vrednostima emisije
Primena instrumentalnih metoda na analizu uzoraka vode Zoran Simi ć, master inženjer tehnologije Tehnološko-metalurški fakultet Univerziteta u Beogradu, Beograd 1 Uredba o granicnim vrednostima emisije
Microsoft Word - PRIJEMNI ISPIT DOC
 Универзитет у Бања Луци Бања Лука, 2009.г. ОЈ Природно-математички факултет Студијски програм Екологија и заштита животне средине Име и презиме кандидата: ПРИЈЕМНИ ИСПИТ БИОЛОГИЈА Заокружите слово испред
Универзитет у Бања Луци Бања Лука, 2009.г. ОЈ Природно-математички факултет Студијски програм Екологија и заштита животне средине Име и презиме кандидата: ПРИЈЕМНИ ИСПИТ БИОЛОГИЈА Заокружите слово испред
Alkeni ili olefini – CnH2n
 ALKENI ili olefini C n H 2n Sadrže dvostruku C=C vezu Važan strukturni elemenat i funkcionalna grupa u organskoj hemiji Oblik molekule uvjetovan je prisustvom ove veze Dvostruka veza je mjesto na kojem
ALKENI ili olefini C n H 2n Sadrže dvostruku C=C vezu Važan strukturni elemenat i funkcionalna grupa u organskoj hemiji Oblik molekule uvjetovan je prisustvom ove veze Dvostruka veza je mjesto na kojem
Microsoft PowerPoint - 4_Hemijska_korozija.ppt - Compatibility Mode
 KOROZIJA I ZAŠTITA METALA dr Aleksandar Lj. Bojić Hemijska korozija metala 1 Hemijska korozija: proces reagovanja metalne površine sa okolinom, kod koga je prelaz metala u jonsko stanje i redukcija oksidacione
KOROZIJA I ZAŠTITA METALA dr Aleksandar Lj. Bojić Hemijska korozija metala 1 Hemijska korozija: proces reagovanja metalne površine sa okolinom, kod koga je prelaz metala u jonsko stanje i redukcija oksidacione
Slide 1
 Kompleksi Prelazni metali Međusobno imaju slične osobine Dosta se razlikuju od alkalih i zemnoalkalnih metala Imaju visoku tačku topljenja,veliku gustinu, uglavnom veliku tvrdoću, dobri su provodnici
Kompleksi Prelazni metali Međusobno imaju slične osobine Dosta se razlikuju od alkalih i zemnoalkalnih metala Imaju visoku tačku topljenja,veliku gustinu, uglavnom veliku tvrdoću, dobri su provodnici
Прилог 7. Граничне вредности концентрације опасних компоненти у отпаду на основу којих се одређују карактеристике отпада (својства отпада која га кара
 Прилог 7. Граничне вредности концентрације опасних компоненти у отпаду на основу којих се одређују карактеристике отпада (својства отпада која га карактеришу као опасан отпад) H1 Експлозиван : Отпад класификован
Прилог 7. Граничне вредности концентрације опасних компоненти у отпаду на основу којих се одређују карактеристике отпада (својства отпада која га карактеришу као опасан отпад) H1 Експлозиван : Отпад класификован
BELANČEVINE MLEKA
 ENZIMI Dr Radoslava Savić Radovanović, docent Enzimi u mleku Endogeni enzimi (enzimi koji potiču iz mlečne žlezde) Poreklom iz ćelija mlečne žlezde, Poreklom iz somatskih ćelija Enzimi poreklom iz mikroorganizama.
ENZIMI Dr Radoslava Savić Radovanović, docent Enzimi u mleku Endogeni enzimi (enzimi koji potiču iz mlečne žlezde) Poreklom iz ćelija mlečne žlezde, Poreklom iz somatskih ćelija Enzimi poreklom iz mikroorganizama.
Slide 1
 Utjecaj ciljane gnojidbe na povećanje randmana i kvalitativna svojstva maslinovog ulja. 4. FESTIVAL MASLINA Zagreb, 23.-24. veljače 2019. Autorica: mr.sc. Sanja Biškup MINERALNA GNOJIVA nastaju od prirodnih
Utjecaj ciljane gnojidbe na povećanje randmana i kvalitativna svojstva maslinovog ulja. 4. FESTIVAL MASLINA Zagreb, 23.-24. veljače 2019. Autorica: mr.sc. Sanja Biškup MINERALNA GNOJIVA nastaju od prirodnih
ОПШТА И НЕОРГАНСКА ХЕМИЈА ИНТЕГРИСАНЕ АКАДЕМСКЕ СТУДИЈЕ ФАРМАЦИЈЕ ПРВА ГОДИНА СТУДИЈА школска 2015/2016.
 ОПШТА И НЕОРГАНСКА ХЕМИЈА ИНТЕГРИСАНЕ АКАДЕМСКЕ СТУДИЈЕ ФАРМАЦИЈЕ ПРВА ГОДИНА СТУДИЈА школска 2015/2016. Предмет: ОПШТА И НЕОРГАНСКА ХЕМИЈА Предмет се вреднује са 9 ЕСПБ. Недељно има 6 часова активне
ОПШТА И НЕОРГАНСКА ХЕМИЈА ИНТЕГРИСАНЕ АКАДЕМСКЕ СТУДИЈЕ ФАРМАЦИЈЕ ПРВА ГОДИНА СТУДИЈА школска 2015/2016. Предмет: ОПШТА И НЕОРГАНСКА ХЕМИЈА Предмет се вреднује са 9 ЕСПБ. Недељно има 6 часова активне
Microsoft PowerPoint - Šesti tjedan.pptx
 REKCIJSKO INŽENJERSTVO I KTLIZ KINETIK i MEHNIZM HOMOGENO KTLITIČKIH REKCIJ Vanja Kosar, izv. prof. Kod homogene katalize, reaktanti, produkti i katalizator nalaze se u istom agregatnom stanju Brzina homogeno
REKCIJSKO INŽENJERSTVO I KTLIZ KINETIK i MEHNIZM HOMOGENO KTLITIČKIH REKCIJ Vanja Kosar, izv. prof. Kod homogene katalize, reaktanti, produkti i katalizator nalaze se u istom agregatnom stanju Brzina homogeno
Microsoft Word - PRIJEMNI EKOLOGIJA 2013_2.doc
 Универзитет у Бањој Луци Бања Лука 2013.г. ОЈ Природно-математички факултет Студијски програм Екологија и заштита животне средине Име и презиме кандидата: ПРИЈЕМНИ ИСПИТ БИОЛОГИЈА Заокружите слово испред
Универзитет у Бањој Луци Бања Лука 2013.г. ОЈ Природно-математички факултет Студијски програм Екологија и заштита животне средине Име и презиме кандидата: ПРИЈЕМНИ ИСПИТ БИОЛОГИЈА Заокружите слово испред
KEM KEMIJA Ispitna knjižica 2 OGLEDNI ISPIT KEM IK-2 OGLEDNI ISPIT 12 1
 KEM KEMIJA Ispitna knjižica 2 OGLEDNI ISPIT 2 Prazna stranica 99 2 OPĆE UPUTE Pozorno pročitajte sve upute i slijedite ih. Ne okrećite stranicu i ne rješavajte zadatke dok to ne odobri dežurni nastavnik.
KEM KEMIJA Ispitna knjižica 2 OGLEDNI ISPIT 2 Prazna stranica 99 2 OPĆE UPUTE Pozorno pročitajte sve upute i slijedite ih. Ne okrećite stranicu i ne rješavajte zadatke dok to ne odobri dežurni nastavnik.
Microsoft PowerPoint - TPOI_07&08_Halogeniranje & Alkilacija_(produkti) [Compatibility Mode]
![Microsoft PowerPoint - TPOI_07&08_Halogeniranje & Alkilacija_(produkti) [Compatibility Mode] Microsoft PowerPoint - TPOI_07&08_Halogeniranje & Alkilacija_(produkti) [Compatibility Mode]](/thumbs/101/151947582.jpg) Fakultet kemijskog inženjerstva i tehnologije Diplomski studij: Kemijsko inženjerstvo Kolegij: Tehnološki procesi organske industrije Izv. prof. dr. sc. Hrvoje Kušić PROCES HALOGENIRANJA Proces kojim se
Fakultet kemijskog inženjerstva i tehnologije Diplomski studij: Kemijsko inženjerstvo Kolegij: Tehnološki procesi organske industrije Izv. prof. dr. sc. Hrvoje Kušić PROCES HALOGENIRANJA Proces kojim se
Microsoft PowerPoint - 11_Ugljenik_Silicijum_Kalaj_Olovo [Compatibility Mode]
![Microsoft PowerPoint - 11_Ugljenik_Silicijum_Kalaj_Olovo [Compatibility Mode] Microsoft PowerPoint - 11_Ugljenik_Silicijum_Kalaj_Olovo [Compatibility Mode]](/thumbs/101/152254832.jpg) 14. GRUPA PERIODNOG SISTEMA 14. GRUPA PERIODNOG SISTEMA Ugljenik na 16. mestu po rasprostranjenosti: u obliku karbonata, fosilnih goriva (uglja, nafte, prirodnog gasa), CO2 i veoma retko u elementarnom
14. GRUPA PERIODNOG SISTEMA 14. GRUPA PERIODNOG SISTEMA Ugljenik na 16. mestu po rasprostranjenosti: u obliku karbonata, fosilnih goriva (uglja, nafte, prirodnog gasa), CO2 i veoma retko u elementarnom
Prezentacja programu PowerPoint
 Aromatski ugljikovodici benzen II dio Karakterističan tip reakcije benzena i njegovih derivata. Benzen podliježe reakciji supstitucije u prisustvu elektrofilne čestice ("+" naelektrisana čestica kod koje
Aromatski ugljikovodici benzen II dio Karakterističan tip reakcije benzena i njegovih derivata. Benzen podliježe reakciji supstitucije u prisustvu elektrofilne čestice ("+" naelektrisana čestica kod koje
ХЕМИЈСКИ ЗАКОНИ 1. Сумпор и кисеоник граде два оксида у којима су масени односи 1 : 1 и 2 : 3. Колика је минимална маса кисеоника потребна за потпуно
 ХЕМИЈСКИ ЗАКОНИ 1. Сумпор и кисеоник граде два оксида у којима су масени односи 1 : 1 и 2 : 3. Колика је минимална маса кисеоника потребна за потпуно сагоравање 32 g сумпора? Написати формулу насталог
ХЕМИЈСКИ ЗАКОНИ 1. Сумпор и кисеоник граде два оксида у којима су масени односи 1 : 1 и 2 : 3. Колика је минимална маса кисеоника потребна за потпуно сагоравање 32 g сумпора? Написати формулу насталог
Republika Hrvatska - Ministarstvo znanosti, obrazovanja i sporta Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEM
 Republika Hrvatska - Ministarstvo znanosti, obrazovanja i sporta Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEMIJE učeni(ka)ca osnovnih i srednjih škola 2013. PISANA
Republika Hrvatska - Ministarstvo znanosti, obrazovanja i sporta Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEMIJE učeni(ka)ca osnovnih i srednjih škola 2013. PISANA
Microsoft Word - dopuna konkursne dok hemikalije -4.doc
 ЗАВОД ЗА ЈАВНО ЗДРАВЉЕ УЖИЦЕ др.в.маринковића бр. 4, 31000 Ужице (031) 563-150, факс: (031) 563-147 e-mail: zzzzu@eunet.rs Датум: 04.09.2015. Предмет: Измена конкурсне документације бр. 4387 oд 11.08.2015.
ЗАВОД ЗА ЈАВНО ЗДРАВЉЕ УЖИЦЕ др.в.маринковића бр. 4, 31000 Ужице (031) 563-150, факс: (031) 563-147 e-mail: zzzzu@eunet.rs Датум: 04.09.2015. Предмет: Измена конкурсне документације бр. 4387 oд 11.08.2015.
Republika Hrvatska - Ministarstvo znanosti, obrazovanja i športa - Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŽUPANIJSKO NATJECANJE I
 Republika Hrvatska - Ministarstvo znanosti, obrazovanja i športa - Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŽUPANIJSKO NATJECANJE IZ KEMIJE učenika osnovnih i srednjih škola 009. PISANA
Republika Hrvatska - Ministarstvo znanosti, obrazovanja i športa - Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŽUPANIJSKO NATJECANJE IZ KEMIJE učenika osnovnih i srednjih škola 009. PISANA
ALKALITET VODE (p i m-vrijednost) Ukupnu tvrdoću sačinjavaju sve kalcijeve i magnezijeve soli sadržane u vodi u obliku karbonata, hidrogenkarbonata, k
 ALKALITET VODE (p i m-vrijednost) Ukupnu tvrdoću sačinjavaju sve kalcijeve i magnezijeve soli sadržane u vodi u obliku karbonata, hidrogenkarbonata, klorida, sulfata, nitrata, silikata, fosfata i dr. Iz
ALKALITET VODE (p i m-vrijednost) Ukupnu tvrdoću sačinjavaju sve kalcijeve i magnezijeve soli sadržane u vodi u obliku karbonata, hidrogenkarbonata, klorida, sulfata, nitrata, silikata, fosfata i dr. Iz
Diapositive 1
 KARBOHIDROGENI (UGLJIKOVODICI) ALIFATSKI AROMATSKI CIKLIČKI ACIKLIČKI ALKANI ALKENI ALKINI Alkani Sadrže samo C i H Opća formula C n H 2n+2 Svi C atomi su sp 3 hibridizirani U molekulama se nalaze samo
KARBOHIDROGENI (UGLJIKOVODICI) ALIFATSKI AROMATSKI CIKLIČKI ACIKLIČKI ALKANI ALKENI ALKINI Alkani Sadrže samo C i H Opća formula C n H 2n+2 Svi C atomi su sp 3 hibridizirani U molekulama se nalaze samo
Katolički školski centar Sv. Josip Sarajevo Srednja medicinska škola ISPITNI KATALOG ZA ZAVRŠNI ISPIT IZ KEMIJE U ŠKOLSKOJ / GODINI Predme
 Katolički školski centar Sv. Josip Sarajevo Srednja medicinska škola ISPITNI KATALOG ZA ZAVRŠNI ISPIT IZ KEMIJE U ŠKOLSKOJ 2017. / 2018. GODINI Predmetno povjerenstvo za kemiju: Antonija Almaš - Ivković,
Katolički školski centar Sv. Josip Sarajevo Srednja medicinska škola ISPITNI KATALOG ZA ZAVRŠNI ISPIT IZ KEMIJE U ŠKOLSKOJ 2017. / 2018. GODINI Predmetno povjerenstvo za kemiju: Antonija Almaš - Ivković,
PowerPoint Presentation
 Prečišćavanje otpadnih gasova Pregled SISTEMI ZA PREČIŠĆAVANJE OTPADNIH GASOVA SISTEMI ZA UKLANJANJE ČESTICA SISTEMI ZA UKLANJANJE GASOVITIH POLUTANATA 10 Emisija u svetu (Mt/god) CO VOCs SOx NOx ČESTICE
Prečišćavanje otpadnih gasova Pregled SISTEMI ZA PREČIŠĆAVANJE OTPADNIH GASOVA SISTEMI ZA UKLANJANJE ČESTICA SISTEMI ZA UKLANJANJE GASOVITIH POLUTANATA 10 Emisija u svetu (Mt/god) CO VOCs SOx NOx ČESTICE
Osnove organske hemije Alkeni, nomenklatura, dobivanje i reakcije
 Osnove organske hemije Alkeni, nomenklatura, dobivanje i reakcije Opšta formula C n H 2n Nastavak je en Alkeni Funkcionalna grupa: C=C veza. Nezasićeni ugljikovodici podliježu reakcijama adicije. Prvi
Osnove organske hemije Alkeni, nomenklatura, dobivanje i reakcije Opšta formula C n H 2n Nastavak je en Alkeni Funkcionalna grupa: C=C veza. Nezasićeni ugljikovodici podliježu reakcijama adicije. Prvi
Microsoft Word - prijemni_08.doc
 Univerzitet u Banjoj Luci Prirodno-matematički fakultet Banja Luka, 2008.g, ODSJEK ZA EKOLOGIJU I ZAŠTITU ŽIVOTNE SREDINE Ime i prezime kandidata KVALIFIKACIONI ISPIT BIOLOGIJA Zaokružite slovo ispred
Univerzitet u Banjoj Luci Prirodno-matematički fakultet Banja Luka, 2008.g, ODSJEK ZA EKOLOGIJU I ZAŠTITU ŽIVOTNE SREDINE Ime i prezime kandidata KVALIFIKACIONI ISPIT BIOLOGIJA Zaokružite slovo ispred
Naknade za poslove Centra za vinogradarstvo, vinarstvo i uljarstvo koje su propisane pravilnikom Redni broj NAZIV PROPISA broj Narodnih Novina 1. Prav
 Naknade za poslove Centra za vinogradarstvo, vinarstvo i uljarstvo koje su propisane pravilnikom Redni broj NAZIV PROPISA broj Narodnih Novina 1. Pravilnik o visini naknade troškova za obavljanje usluga
Naknade za poslove Centra za vinogradarstvo, vinarstvo i uljarstvo koje su propisane pravilnikom Redni broj NAZIV PROPISA broj Narodnih Novina 1. Pravilnik o visini naknade troškova za obavljanje usluga
Microsoft PowerPoint - 3_Elektrohemijska_korozija_kinetika.ppt - Compatibility Mode
 KOROZIJA I ZAŠTITA METALA dr Aleksandar Lj. Bojić Elektrohemijska korozija Kinetika korozionog procesa 1 Korozioni sistem izvan stanja ravnoteže polarizacija Korozija metala: istovremeno odvijanje dve
KOROZIJA I ZAŠTITA METALA dr Aleksandar Lj. Bojić Elektrohemijska korozija Kinetika korozionog procesa 1 Korozioni sistem izvan stanja ravnoteže polarizacija Korozija metala: istovremeno odvijanje dve
PowerPoint Presentation
 OSNOVE ORGANSKE HEMIJE Šta je to organska hemija i zašto je proučavamo Organska hemija ili Svijet ugljika/karbona Organske supstance (npr. maslinovo ulje, šeder, škrob, svila, guma, papir, penicilin )
OSNOVE ORGANSKE HEMIJE Šta je to organska hemija i zašto je proučavamo Organska hemija ili Svijet ugljika/karbona Organske supstance (npr. maslinovo ulje, šeder, škrob, svila, guma, papir, penicilin )
ALKOHOLI
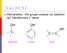 ALKLI Hidroksilna grupa vezana na zasićeni sp 3 hibridizirani C-atom C C C Alkohol Fenol Enol Alkoholi u prirodi CH 3 CH 3 CH 2 Etanol CH3 Metanol CH 3 CH 3 Mentol (iz pepermint ulja) Izoprenska jedinica
ALKLI Hidroksilna grupa vezana na zasićeni sp 3 hibridizirani C-atom C C C Alkohol Fenol Enol Alkoholi u prirodi CH 3 CH 3 CH 2 Etanol CH3 Metanol CH 3 CH 3 Mentol (iz pepermint ulja) Izoprenska jedinica
Prezentacja programu PowerPoint
 Aromatski ugljikovodici benzen Vanilin je esencijalna komponenta ulja vanilije dobivenog iz orhideje Vanilla fragrans. To je drugi najskuplji začin (poslije šafrana) Benzaldehid (iz višanja, breskvi,
Aromatski ugljikovodici benzen Vanilin je esencijalna komponenta ulja vanilije dobivenog iz orhideje Vanilla fragrans. To je drugi najskuplji začin (poslije šafrana) Benzaldehid (iz višanja, breskvi,
Republika Hrvatska - Ministarstvo znanosti, obrazovanja i športa
 Republika Hrvatska - Ministarstvo znanosti, obrazovanja i športa Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEMIJE učeni(ka)ca osnovnih i srednjih škola 2011. PISANA
Republika Hrvatska - Ministarstvo znanosti, obrazovanja i športa Agencija za odgoj i obrazovanje - Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEMIJE učeni(ka)ca osnovnih i srednjih škola 2011. PISANA
Microsoft PowerPoint - 2_Elhem_kor_principi i termodinamika.pptx
 KOROZIJA I ZAŠTITA METALA dr Aleksandar Lj. Bojić Principi elektrohemijske korozije 1 Definicija elektrohemijske korozije (HRN EN ISO 8044) Elektrohemijska korozija je korozija koja se odvija putem barem
KOROZIJA I ZAŠTITA METALA dr Aleksandar Lj. Bojić Principi elektrohemijske korozije 1 Definicija elektrohemijske korozije (HRN EN ISO 8044) Elektrohemijska korozija je korozija koja se odvija putem barem
OBIM AKREDITACIJE
 АКРЕДИТАЦИОНО ТЕЛО СРБИЈЕ : Датум прве акредитације/ Date of initial accreditation: 05.11.2010. Ознака предмета/file Ref. No.: 2-01-384 Важи од/ Valid from: Замењује Обим од: Replaces Scope dated: ОБИМ
АКРЕДИТАЦИОНО ТЕЛО СРБИЈЕ : Датум прве акредитације/ Date of initial accreditation: 05.11.2010. Ознака предмета/file Ref. No.: 2-01-384 Важи од/ Valid from: Замењује Обим од: Replaces Scope dated: ОБИМ
DEFINICIJA MLEKA HEMIJSKI SASTAV MLEKA: VODA, MLEČNA MAST, LAKTOZA
 Prof. dr Snežana Bulajić KATEDRA ZA HIGIJENU I TEHNOLOGIJU NAMIRNICA ANIMALNOG POREKLA Mleko je proizvod mlečne žlezde dobijen pravilnom (neprekidna i potpuna muža) i redovnom mužom* zdravih, ispravno
Prof. dr Snežana Bulajić KATEDRA ZA HIGIJENU I TEHNOLOGIJU NAMIRNICA ANIMALNOG POREKLA Mleko je proizvod mlečne žlezde dobijen pravilnom (neprekidna i potpuna muža) i redovnom mužom* zdravih, ispravno
MAŠINSKI MATERIJALI (4+2) Školska h I Nastavna grupa Predmetni nastavnik: Dr Vukić Lazić, red. prof. Saradnici na pre
 MAŠINSKI MATERIJALI (4+2) Školska 2012-13 03. 10. 2012. 8 00 12 00 h I Nastavna grupa Predmetni nastavnik: Dr Vukić Lazić, red. prof. Saradnici na predmetu: Dr Srbislav Aleksandrović, red. prof. Saradnici
MAŠINSKI MATERIJALI (4+2) Školska 2012-13 03. 10. 2012. 8 00 12 00 h I Nastavna grupa Predmetni nastavnik: Dr Vukić Lazić, red. prof. Saradnici na predmetu: Dr Srbislav Aleksandrović, red. prof. Saradnici
505
 505. На основу члана 11 став 3 Закона о заштити ваздуха ( Службени лист ЦГ", број 25/10), Влада Црне Горе на сједници од 8.јула 2010. године, донијела је УРЕДБУ О УСПОСТАВЉАЊУ МРЕЖЕ МЈЕРНИХ МЈЕСТА ЗА ПРАЋЕЊЕ
505. На основу члана 11 став 3 Закона о заштити ваздуха ( Службени лист ЦГ", број 25/10), Влада Црне Горе на сједници од 8.јула 2010. године, донијела је УРЕДБУ О УСПОСТАВЉАЊУ МРЕЖЕ МЈЕРНИХ МЈЕСТА ЗА ПРАЋЕЊЕ
Napomena: Radni spisak je smernica za lakše povezivanje propisa kojim se uređuje promet lekova i medicinskih sredstava sa Nomenklaturom CT i podložan
 Списак супстанци за производњу и промет лекова и, за чији увоз/извоз је потребно прибавити дозволу за производњу лека/медицинског средства на велико или дозволу за промет лека/медицинског средства на велико,
Списак супстанци за производњу и промет лекова и, за чији увоз/извоз је потребно прибавити дозволу за производњу лека/медицинског средства на велико или дозволу за промет лека/медицинског средства на велико,
Fizičko-hemijske karakteristike zagađujućih supstanci
 FIZIČKO-HEMIJSKE KARAKTERISTIKE ZAGAĐUJUĆIH SUPSTANCI Prvo predavanje 1 ŠTA PROUČAVA HEMODINAMIKA ZAGAĐUJUĆIH SUPSTANCI Proces transporta supstanci u životnoj sredini Proces prelaska supstanci između faza
FIZIČKO-HEMIJSKE KARAKTERISTIKE ZAGAĐUJUĆIH SUPSTANCI Prvo predavanje 1 ŠTA PROUČAVA HEMODINAMIKA ZAGAĐUJUĆIH SUPSTANCI Proces transporta supstanci u životnoj sredini Proces prelaska supstanci između faza
Broj: /17 Zagreb, SVEUČILIŠTE U ZAGREBU AGRONOMSKI FAKULTET Oznaka: OB-022 ZAVOD ZA ISHRANU BILJA Izdanje: 02 ANALITIČKI LABORATORIJ
 Stranica: 1/6 VODOVOD I KAALIZACIJA d.o.o. Ogulin, I.G. Kovačića 14 47300 OGULI Rezultati kemijske analize mulja sa uređaja za pročišćavanje otpadnih voda grada Ogulina Poštovani, provedena je kemijska
Stranica: 1/6 VODOVOD I KAALIZACIJA d.o.o. Ogulin, I.G. Kovačića 14 47300 OGULI Rezultati kemijske analize mulja sa uređaja za pročišćavanje otpadnih voda grada Ogulina Poštovani, provedena je kemijska
FENOLI
 FENLI FENLI imaju grupu direktno vezanu na benzenov prsten i spadaju u ARMATSKE SPJEVE. Naziv fenol koristi se i za specifičan spoj, C 6 H 5 i za cijelu klasu spojeva. Sam FENL, otkriven je 1834. god.
FENLI FENLI imaju grupu direktno vezanu na benzenov prsten i spadaju u ARMATSKE SPJEVE. Naziv fenol koristi se i za specifičan spoj, C 6 H 5 i za cijelu klasu spojeva. Sam FENL, otkriven je 1834. god.
БИОНЕОРГАНСКА ХЕМИЈА ИНТЕГРИСАНЕ АКАДЕМСКЕ СТУДИЈЕ ФАРМАЦИЈЕ ТРЕЋА ГОДИНА СТУДИЈА школска 2018/2019.
 БИОНЕОРГАНСКА ХЕМИЈА ИНТЕГРИСАНЕ АКАДЕМСКЕ СТУДИЈЕ ФАРМАЦИЈЕ ТРЕЋА ГОДИНА СТУДИЈА школска 2018/2019. Предмет: БИОНЕОРГАНСКА ХЕМИЈА Предмет се вреднује са 7 ЕСПБ. Недељно има 5 часова активне наставе (2
БИОНЕОРГАНСКА ХЕМИЈА ИНТЕГРИСАНЕ АКАДЕМСКЕ СТУДИЈЕ ФАРМАЦИЈЕ ТРЕЋА ГОДИНА СТУДИЈА школска 2018/2019. Предмет: БИОНЕОРГАНСКА ХЕМИЈА Предмет се вреднује са 7 ЕСПБ. Недељно има 5 часова активне наставе (2
Microsoft Word - Molekuli-zadaci.doc
 Задаци Други колоквијум - Молекулски спектри Пример 1 Израчунајте апсорбанцију раствора, ако је познато да је транспаренција 89% на 00 nm. А 0,071 λ 00 nm таласна дужина на којој је мерена апсорбанција
Задаци Други колоквијум - Молекулски спектри Пример 1 Израчунајте апсорбанцију раствора, ако је познато да је транспаренција 89% на 00 nm. А 0,071 λ 00 nm таласна дужина на којој је мерена апсорбанција
Microsoft PowerPoint - TOR GENERATOR - prezentacija [Compatibility Mode]
![Microsoft PowerPoint - TOR GENERATOR - prezentacija [Compatibility Mode] Microsoft PowerPoint - TOR GENERATOR - prezentacija [Compatibility Mode]](/thumbs/88/116343284.jpg) TEHNOLOGIJA HIDROSTABILIZACIJE TEČNIH GORIVA NA BAZI UGLJOVODONIKA Manje mazuta Više čistog vazduha Manje mazuta Više profita NAJVEĆI ZAGAĐIVAČI VAZDUHA Saobraćaj Termoelektrane Industrija (posebno hemijska)
TEHNOLOGIJA HIDROSTABILIZACIJE TEČNIH GORIVA NA BAZI UGLJOVODONIKA Manje mazuta Više čistog vazduha Manje mazuta Više profita NAJVEĆI ZAGAĐIVAČI VAZDUHA Saobraćaj Termoelektrane Industrija (posebno hemijska)
Weishaupt monarch (WM) serija
 Gorionici - uštede energije primenom O2 i frekventne regulacije Emisije štetnih materija u produktima sagorevanja Budva, 23.09.2016. Gorionici Uštede energije O 2 regulacija ušteda minimum 2% goriva vraćanje
Gorionici - uštede energije primenom O2 i frekventne regulacije Emisije štetnih materija u produktima sagorevanja Budva, 23.09.2016. Gorionici Uštede energije O 2 regulacija ušteda minimum 2% goriva vraćanje
Правилник o допунама Правилника о ограничењима и забранама производње, стављања у промет и коришћења хемикалија Члан 1. У Правилнику о ограничењима и
 Правилник o допунама Правилника о ограничењима и забранама производње, стављања у промет и коришћења хемикалија Члан 1. У Правилнику о ограничењима и забранама производње, стављања у промет и коришћења
Правилник o допунама Правилника о ограничењима и забранама производње, стављања у промет и коришћења хемикалија Члан 1. У Правилнику о ограничењима и забранама производње, стављања у промет и коришћења
naslovnica_zup_2017
 Republika rvatska - Ministarstvo znanosti i obrazovanja Agencija za odgoj i obrazovanje - rvatsko kemijsko društvo ŽUPANIJSKO NATJECANJE IZ KEMIJE učenika osnovnih i srednjih škola 2017. PISANA ZADAĆA
Republika rvatska - Ministarstvo znanosti i obrazovanja Agencija za odgoj i obrazovanje - rvatsko kemijsko društvo ŽUPANIJSKO NATJECANJE IZ KEMIJE učenika osnovnih i srednjih škola 2017. PISANA ZADAĆA
Bor, Srbija GEOLOGIJA MINERALNIH LEŽIŠTA Andrea Čobić
 Bor, Srbija GEOLOGIJA MINERALNIH LEŽIŠTA Andrea Čobić (ancobic@geol.pmf.hr) Sadržaj kolegija Ekonomski aspekt mineralnih ležišta Analitičke metode u istraživanjima mineralnih ležišta Teksture i strukture
Bor, Srbija GEOLOGIJA MINERALNIH LEŽIŠTA Andrea Čobić (ancobic@geol.pmf.hr) Sadržaj kolegija Ekonomski aspekt mineralnih ležišta Analitičke metode u istraživanjima mineralnih ležišta Teksture i strukture
IPPC zahtev[1] [Compatibility Mode]
![IPPC zahtev[1] [Compatibility Mode] IPPC zahtev[1] [Compatibility Mode]](/thumbs/102/154561259.jpg) ПРИМЕНА IPPC ДИРЕКТИВЕ У СРБИЈИ ЗАХТЕВ ЗА ИЗДАВАЊЕ ИНТЕГРИСАНЕ ДОЗВОЛЕ qзакон о интегрисаном спречавању и контроли загађивања животне средине (Сл. Гласник РС, број 135/2004) Уређује услове и поступак издавања
ПРИМЕНА IPPC ДИРЕКТИВЕ У СРБИЈИ ЗАХТЕВ ЗА ИЗДАВАЊЕ ИНТЕГРИСАНЕ ДОЗВОЛЕ qзакон о интегрисаном спречавању и контроли загађивања животне средине (Сл. Гласник РС, број 135/2004) Уређује услове и поступак издавања
13 Jul Plantaže a.d. Podgorica Broj: 2341/19/1 Redni broj iz Plana nabavki: 7 Mjesto i datum: Podgorica, g. ZAHTJEV ZA PRIKUPLJANJE PONUDA
 13 Jul Plantaže a.d. Podgorica Broj: 2341/19/1 Redni broj iz Plana nabavki: 7 Mjesto i datum: Podgorica, 18.04.2019.g. ZAHTJEV ZA PRIKUPLJANJE PONUDA ZA POSTUPAK NABAVKE SREDSTAVA ZA KOREKCIJU VINA strana
13 Jul Plantaže a.d. Podgorica Broj: 2341/19/1 Redni broj iz Plana nabavki: 7 Mjesto i datum: Podgorica, 18.04.2019.g. ZAHTJEV ZA PRIKUPLJANJE PONUDA ZA POSTUPAK NABAVKE SREDSTAVA ZA KOREKCIJU VINA strana
ANALITIČKA KEMIJA SEMINAR
 SMINAR IZ KOLGIJA ANALITIČKA KMIJA I Studij Primijenjena kemija 1. Izračunajte potenijale sistema H AsO H AsO pri ph 1 i ph 6 u trenutku kada su konentraije oksidiranog i reduiranog oblika izjednačene!
SMINAR IZ KOLGIJA ANALITIČKA KMIJA I Studij Primijenjena kemija 1. Izračunajte potenijale sistema H AsO H AsO pri ph 1 i ph 6 u trenutku kada su konentraije oksidiranog i reduiranog oblika izjednačene!
KARBOKSILNE KISELINE
 Najvažnije nezasićene dikarbonske kiseline su maleinska i fumarna kiselina kao klasični primjeri geometrijske izomerije tzv. cis- i transizomerija: H C HC C H H C H C cis-maleinska kiselina trans-fumarna
Najvažnije nezasićene dikarbonske kiseline su maleinska i fumarna kiselina kao klasični primjeri geometrijske izomerije tzv. cis- i transizomerija: H C HC C H H C H C cis-maleinska kiselina trans-fumarna
INOVATIVNI POSTUPAK SINTEZE VISOKO EFIKASNOG ADSORPCIONOG MATERIJALA ZA UKLANJANJE KADMIJUM(II) JONA NA BAZI VINIL MODIFIKOVANOG LIGNINA Ana POPOVIĆ,
 INOVATIVNI POSTUPAK SINTEZE VISOKO EFIKASNOG ADSORPCIONOG MATERIJALA ZA UKLANJANJE KADMIJUM(II) JONA NA BAZI VINIL MODIFIKOVANOG LIGNINA Ana POPOVIĆ, Jelena RUSMIROVIĆ, Željko RADOVANOVIĆ, Milena MILOŠEVIĆ,
INOVATIVNI POSTUPAK SINTEZE VISOKO EFIKASNOG ADSORPCIONOG MATERIJALA ZA UKLANJANJE KADMIJUM(II) JONA NA BAZI VINIL MODIFIKOVANOG LIGNINA Ana POPOVIĆ, Jelena RUSMIROVIĆ, Željko RADOVANOVIĆ, Milena MILOŠEVIĆ,
Microsoft PowerPoint - 14obk-s11a-uvod u metabolizam
 Seminar 11a Uvod u metabolizam Boris Mildner Rješenja zadaće 10. 1. D 11. D 2. B 12. B 3. B 13. C 4. A 14. A 5. A 15. B 6. B 16. B 7. D 17. D 8. A 18. B 9. C 19. D 10. B 20. D 1 1. Koji enzim u želucu
Seminar 11a Uvod u metabolizam Boris Mildner Rješenja zadaće 10. 1. D 11. D 2. B 12. B 3. B 13. C 4. A 14. A 5. A 15. B 6. B 16. B 7. D 17. D 8. A 18. B 9. C 19. D 10. B 20. D 1 1. Koji enzim u želucu
Republika Hrvatska Ministarstvo znanosti i obrazovanja Agencija za odgoj i obrazovanje Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEMIJE učenika
 Republika Hrvatska Ministarstvo znanosti i obrazovanja Agencija za odgoj i obrazovanje Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEMIJE učenika osnovnih i srednjih škola 019. PISANA ZADAĆA NAPOMENA:
Republika Hrvatska Ministarstvo znanosti i obrazovanja Agencija za odgoj i obrazovanje Hrvatsko kemijsko društvo ŠKOLSKO NATJECANJE IZ KEMIJE učenika osnovnih i srednjih škola 019. PISANA ZADAĆA NAPOMENA:
Microsoft Word - knjiga 3
 Strana 1 od 435 OPŠTINA: OBRENOVAC/Stubline Broj i oznaka objekta: ST220 Datum uzorkovanja: 03.10.2010 Vlasnik objekta: Vasić Steva Koordinate: N: 44.57440 E: 20.13583 Skica lokaliteta: Adresa: k.br. Stubline
Strana 1 od 435 OPŠTINA: OBRENOVAC/Stubline Broj i oznaka objekta: ST220 Datum uzorkovanja: 03.10.2010 Vlasnik objekta: Vasić Steva Koordinate: N: 44.57440 E: 20.13583 Skica lokaliteta: Adresa: k.br. Stubline
Narodne novine, broj 162/98. i 107/07. ZAKON O LISTI PROFESIONALNIH BOLESTI (neslužbeno pročišćeni tekst) Članak 1. Ovim se Zakonom utvrđuju bolesti k
 Narodne novine, broj 162/98. i 107/07. ZAKON O LISTI PROFESIONALNIH BOLESTI (neslužbeno pročišćeni tekst) Članak 1. Ovim se Zakonom utvrđuju bolesti koje se, prema članku 38. stavku 1. Zakona o mirovinskom
Narodne novine, broj 162/98. i 107/07. ZAKON O LISTI PROFESIONALNIH BOLESTI (neslužbeno pročišćeni tekst) Članak 1. Ovim se Zakonom utvrđuju bolesti koje se, prema članku 38. stavku 1. Zakona o mirovinskom
MEHANIZAM DJELOVANJA ALKOHOL DEHIDROGENAZE
 MEHANIZAM DJELOVANJA ALKOHOL DEHIDROGENAZE Viktorija Medvarić Skupina oksidoreduktaza (E.C. 1.1.1.1) Koenzim NAD(P)H Interkonverzija alkohola u aldehid/keton U arhejama, bakterijama i eukariotima Tip I,
MEHANIZAM DJELOVANJA ALKOHOL DEHIDROGENAZE Viktorija Medvarić Skupina oksidoreduktaza (E.C. 1.1.1.1) Koenzim NAD(P)H Interkonverzija alkohola u aldehid/keton U arhejama, bakterijama i eukariotima Tip I,
NATIONALE SCHEIKUNDEOLYMPIADE
 Вода и одрживост Теоријски задаци Лист за одговоре 7. децембар 2017. Концентрација кисеоника (µmol/l) Биологија - задаци Биљни свет у поплављеним равницама 1. Користите график са вашег листа за одговоре
Вода и одрживост Теоријски задаци Лист за одговоре 7. децембар 2017. Концентрација кисеоника (µmol/l) Биологија - задаци Биљни свет у поплављеним равницама 1. Користите график са вашег листа за одговоре
1621. Na osnovu člana 64 stav 4 Zakona o bezbjednosti hrane ( Službeni list CG, broj 57/15), Vlada Crne Gore, na sjednici od 2. decembra godine,
 1621. Na osnovu člana 64 stav 4 Zakona o bezbjednosti hrane ( Službeni list CG, broj 57/15), Vlada Crne Gore, na sjednici od 2. decembra 2016. godine, donijela je UREDBU O VITAMINIMA, MINERALIMA I DRUGIM
1621. Na osnovu člana 64 stav 4 Zakona o bezbjednosti hrane ( Službeni list CG, broj 57/15), Vlada Crne Gore, na sjednici od 2. decembra 2016. godine, donijela je UREDBU O VITAMINIMA, MINERALIMA I DRUGIM
UNIVERZITET U SARAJEVU PRIRODNO-MATEMATIČKI FAKULTET AMIRA ČOPRA-JANIĆIJEVIĆ LEJLA KLEPO ANELA TOPČAGIĆ PRAKTIKUM ORGANSKE HEMIJE Univerzitetsko izdan
 UNIVERZITET U SARAJEVU PRIRDN-MATEMATIČKI FAKULTET AMIRA ČPRA-JANIĆIJEVIĆ LEJLA KLEP ANELA TPČAGIĆ PRAKTIKUM RGANSKE EMIJE Univerzitetsko izdanje Sarajevo, 2013. godina PRAKTIKUM RGANSKE EMIJE Autori Amira
UNIVERZITET U SARAJEVU PRIRDN-MATEMATIČKI FAKULTET AMIRA ČPRA-JANIĆIJEVIĆ LEJLA KLEP ANELA TPČAGIĆ PRAKTIKUM RGANSKE EMIJE Univerzitetsko izdanje Sarajevo, 2013. godina PRAKTIKUM RGANSKE EMIJE Autori Amira
OKFH2-12
 ELEKTRIČNE OSOBINE Električne osobine atoma i molekula uslovljavaju: ojavu dvojnog relamanja svetlosti ojavu olarizacije rasejane svetlosti dielektrične osobine međumolekulske interakcije ravila izbora
ELEKTRIČNE OSOBINE Električne osobine atoma i molekula uslovljavaju: ojavu dvojnog relamanja svetlosti ojavu olarizacije rasejane svetlosti dielektrične osobine međumolekulske interakcije ravila izbora
OKFH2-10
 KOLOIDI DISPERZNI SISTEMI Disperzni sistemi sistemi u kojima je jedna ili više supstancija (disperzna faza) u većoj ili manjoj meri usitnjena i ravnomerno raspoređena u okružujućoj sredini (disperzno sredstvo).
KOLOIDI DISPERZNI SISTEMI Disperzni sistemi sistemi u kojima je jedna ili više supstancija (disperzna faza) u većoj ili manjoj meri usitnjena i ravnomerno raspoređena u okružujućoj sredini (disperzno sredstvo).
РЕПУБЛИКА СРБИЈА ЗАВОД ЗА ЈАВНО ЗДРАВЉЕ ПОЖАРЕВАЦ Јована Шербановића 14, Пожаревац Web: E- mail: Тел.: 012/222-
 ЦЕНТАР ЗА ХИГИЈЕНУ И ХУМАНУ ЕКОЛОГИЈУ ИЗВЕШТАЈ О КОНТРОЛИ КВАЛИТЕТА ВАЗДУХА У СМЕДЕРЕВУ У 2017. ГОДИНИ јануар 2018 УВОД Завод за јавно здравље Пожаревац је на захтев Министарства заштите животне средине
ЦЕНТАР ЗА ХИГИЈЕНУ И ХУМАНУ ЕКОЛОГИЈУ ИЗВЕШТАЈ О КОНТРОЛИ КВАЛИТЕТА ВАЗДУХА У СМЕДЕРЕВУ У 2017. ГОДИНИ јануар 2018 УВОД Завод за јавно здравље Пожаревац је на захтев Министарства заштите животне средине
Odjel za zdravstvenu ispravnost i kvalitetu hrane i predmeta opće uporabe Služba za zaštitu okoliša i zdravstvenu ekologiju Mirogojska cesta 16, Zagre
 Odjel za zdravstvenu ispravnost i kvalitetu hrane i predmeta opće uporabe Služba za zaštitu okoliša i zdravstvenu ekologiju Mirogojska cesta 16, Zagreb Tel. 01/4696 227, Fax. 01/4678 103 www.stampar.hr
Odjel za zdravstvenu ispravnost i kvalitetu hrane i predmeta opće uporabe Služba za zaštitu okoliša i zdravstvenu ekologiju Mirogojska cesta 16, Zagreb Tel. 01/4696 227, Fax. 01/4678 103 www.stampar.hr
Smernice za iskazivanje obima akreditacije LI
 АТС-УП30 СМЕРНИЦЕ ЗА ИСКАЗИВАЊЕ ОБИМА АКРЕДИТАЦИЈЕ ПРОВАЈДЕРА ПРОГРАМА ЗА ИСПИТИВАЊЕ ОСПОСОБЉЕНОСТИ Овај документ је важећи и без потписа особа које су преиспитале и одобриле документ. Издање/Измена: 1/1
АТС-УП30 СМЕРНИЦЕ ЗА ИСКАЗИВАЊЕ ОБИМА АКРЕДИТАЦИЈЕ ПРОВАЈДЕРА ПРОГРАМА ЗА ИСПИТИВАЊЕ ОСПОСОБЉЕНОСТИ Овај документ је важећи и без потписа особа које су преиспитале и одобриле документ. Издање/Измена: 1/1
1 Vježba 11. ENERGETSKE PROMJENE PRI OTAPANJU SOLI. OVISNOST TOPLJIVOSTI O TEMPERATURI. Uvod: Prilikom otapanja soli u nekom otapalu (najčešće je to v
 1 Vježba 11. ENERGETSKE PROMJENE PRI OTAPANJU SOLI. OVISNOST TOPLJIVOSTI O TEMPERATURI. Uvod: Prilikom otapanja soli u nekom otapalu (najčešće je to voda) istodobno se odvijaju dva procesa. Prvi proces
1 Vježba 11. ENERGETSKE PROMJENE PRI OTAPANJU SOLI. OVISNOST TOPLJIVOSTI O TEMPERATURI. Uvod: Prilikom otapanja soli u nekom otapalu (najčešće je to voda) istodobno se odvijaju dva procesa. Prvi proces
Prilog 3 - Kriterijumi za dodelu Eko znaka za oplemenjivače zemljišta
 Прилог 3 КРИТЕРИЈУМИ ЗА ДОДЕЛУ ЕКО ЗНАКА ЗА ОПЛЕМЕЊИВАЧЕ ЗЕМЉИШТА Критеријуми за доделу Еко знака за оплемењиваче земљишта имају за циљ: 1) употребу обновљивих материјала и/или рециклажу органских материја
Прилог 3 КРИТЕРИЈУМИ ЗА ДОДЕЛУ ЕКО ЗНАКА ЗА ОПЛЕМЕЊИВАЧЕ ЗЕМЉИШТА Критеријуми за доделу Еко знака за оплемењиваче земљишта имају за циљ: 1) употребу обновљивих материјала и/или рециклажу органских материја
Pretvorba metana u metanol korištenjem metalnih oksida
 PRETVORBA METANA U METANOL KORIŠTENJEM METALNIH OKSIDA Ružica Tomašević Kolegij: Anorganski reakcijski mehanizmi Asistent: mag. chem. Vinko Nemec Nositelj kolegija: doc. dr. sc. Vladimir Stilinović 11.
PRETVORBA METANA U METANOL KORIŠTENJEM METALNIH OKSIDA Ružica Tomašević Kolegij: Anorganski reakcijski mehanizmi Asistent: mag. chem. Vinko Nemec Nositelj kolegija: doc. dr. sc. Vladimir Stilinović 11.
Република Србија МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА ЗАВОД ЗА ВРЕДНОВАЊЕ КВАЛИТЕТА ОБРАЗОВАЊА И ВАСПИТАЊА школска 2017/2018. година ТЕС
 Република Србија МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА ЗАВОД ЗА ВРЕДНОВАЊЕ КВАЛИТЕТА ОБРАЗОВАЊА И ВАСПИТАЊА школска 017/018. година ТЕСТ ФИЗИКА ПРИЈЕМНИ ИСПИТ ЗА УПИС УЧЕНИКА СА ПОСЕБНИМ СПОСОБНОСТИМА
Република Србија МИНИСТАРСТВО ПРОСВЕТЕ, НАУКЕ И ТЕХНОЛОШКОГ РАЗВОЈА ЗАВОД ЗА ВРЕДНОВАЊЕ КВАЛИТЕТА ОБРАЗОВАЊА И ВАСПИТАЊА школска 017/018. година ТЕСТ ФИЗИКА ПРИЈЕМНИ ИСПИТ ЗА УПИС УЧЕНИКА СА ПОСЕБНИМ СПОСОБНОСТИМА
Microsoft PowerPoint - SSA_seminar_1_dio [Compatibility Mode]
![Microsoft PowerPoint - SSA_seminar_1_dio [Compatibility Mode] Microsoft PowerPoint - SSA_seminar_1_dio [Compatibility Mode]](/thumbs/100/146475485.jpg) Spektroskopska k k strukturna analiza seminar 1dio 1. nositelj: prof. dr. sc. Predrag Novak održao i sastavio: doc. dr. sc. Tomislav Jednačak; ak. god. 2018./19. Područja kemijskog pomaka signala u 1 H
Spektroskopska k k strukturna analiza seminar 1dio 1. nositelj: prof. dr. sc. Predrag Novak održao i sastavio: doc. dr. sc. Tomislav Jednačak; ak. god. 2018./19. Područja kemijskog pomaka signala u 1 H
БИОХЕМИЈА МЕТАБОЛИЗАМ И ФУНКЦИЈА ДРУГА ГОДИНА СТУДИЈА школска 2018/2019.
 БИОХЕМИЈА МЕТАБОЛИЗАМ И ФУНКЦИЈА ДРУГА ГОДИНА СТУДИЈА школска 2018/2019. Предмет: БИОХЕМИЈА Предмет се вреднује са 15 ЕСПБ. Укупно има 10 часова активне наставе (5 часова предавања и 5 часова вежби недељно).
БИОХЕМИЈА МЕТАБОЛИЗАМ И ФУНКЦИЈА ДРУГА ГОДИНА СТУДИЈА школска 2018/2019. Предмет: БИОХЕМИЈА Предмет се вреднује са 15 ЕСПБ. Укупно има 10 часова активне наставе (5 часова предавања и 5 часова вежби недељно).
Kvadrupolni maseni analizator, princip i primena u kvali/kvanti hromatografiji
 Kvadrupolni maseni analizator, princip i primena u kvali/kvanti hromatografiji doc dr Nenad Vuković, Institut za hemiju, Prirodno-matematički fakultet u Kragujevcu JONIZACIJA ELEKTRONSKIM UDAROM Joni u
Kvadrupolni maseni analizator, princip i primena u kvali/kvanti hromatografiji doc dr Nenad Vuković, Institut za hemiju, Prirodno-matematički fakultet u Kragujevcu JONIZACIJA ELEKTRONSKIM UDAROM Joni u
Kemija prirodnih i sintetskih polimera
 Fakultet kemijskog inženjerstva i tehnologije Sveučilište u Zagrebu Diplomski studij K E M I J S K O I N Ž E NJ E R S T V O - KTP Kolegij: Petrokemijske tehnologije Petrokemija - uvod Prof. dr. sc. Elvira
Fakultet kemijskog inženjerstva i tehnologije Sveučilište u Zagrebu Diplomski studij K E M I J S K O I N Ž E NJ E R S T V O - KTP Kolegij: Petrokemijske tehnologije Petrokemija - uvod Prof. dr. sc. Elvira
Microsoft PowerPoint - IR-Raman1 [Compatibility Mode]
![Microsoft PowerPoint - IR-Raman1 [Compatibility Mode] Microsoft PowerPoint - IR-Raman1 [Compatibility Mode]](/thumbs/101/149990971.jpg) Spektar elektromagnetnoga t zračenja 10 5 10 3 10 1 10-1 10-3 10-5 10-7 E(kJ/mol) 10-6 10-4 10-2 1 10 2 10 4 10-8,cm X UV zrake zrake prijelazi elektrona IR mikrovalovi radiovalovi vibracije rotacije prijelazi
Spektar elektromagnetnoga t zračenja 10 5 10 3 10 1 10-1 10-3 10-5 10-7 E(kJ/mol) 10-6 10-4 10-2 1 10 2 10 4 10-8,cm X UV zrake zrake prijelazi elektrona IR mikrovalovi radiovalovi vibracije rotacije prijelazi
Slide 1
 Univerzitet u Nišu Prirodno-matematički fakultet Departman za hemiju Katedra za neorgansku hemiju Hemija prelaznih metala sa koordinacionom hemijom Školska: 2018/2019. godina Prof. dr Nenad S. Krstić K2_
Univerzitet u Nišu Prirodno-matematički fakultet Departman za hemiju Katedra za neorgansku hemiju Hemija prelaznih metala sa koordinacionom hemijom Školska: 2018/2019. godina Prof. dr Nenad S. Krstić K2_
MINISTARSTVO ZAŠTITE OKOLIŠA I PRIRODE 1746 Na temelju članka 29. stavka 2. Zakona o zaštiti zraka (»Narodne novine«, br. 130/2011, 47/2014), ministar
 INISTARSTVO ZAŠTITE OKOLIŠA I PRIRODE 1746 Na temelju članka 29. stavka 2. Zakona o zaštiti zraka (»Narodne novine«, br. 130/2011, 47/2014), ministar zaštite okoliša i prirode donosi PROGRA JERENJA RAZINE
INISTARSTVO ZAŠTITE OKOLIŠA I PRIRODE 1746 Na temelju članka 29. stavka 2. Zakona o zaštiti zraka (»Narodne novine«, br. 130/2011, 47/2014), ministar zaštite okoliša i prirode donosi PROGRA JERENJA RAZINE
